题目内容
18.有一种线性高分子,结构如图所示.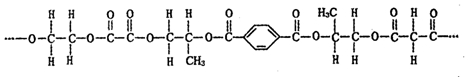
下列有关说法正确的是( )
| A. | 该高分子由4种单体(聚合成髙分子的简单小分子)缩聚而成 | |
| B. | 构成该分子的几种竣酸单体互为同系物 | |
| C. | 上述单体中的乙二醇,可被02催化氧化生成单体之一的草酸 | |
| D. | 该高分子有固定熔沸点,1 mol上述链节完全水解需要氢氧化钠物质的量为 5 mol |
分析 由高聚物可知该有机物的单体有HO-CH2-CH2-OH、HOOC-COOH、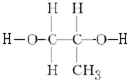 、
、 、HOOC-CH2-COOH等,结合对应有机物的结构和性质解答该题.
、HOOC-CH2-COOH等,结合对应有机物的结构和性质解答该题.
解答 解:A.由高聚物可知该有机物的单体有HO-CH2-CH2-OH、HOOC-COOH、 、
、 、HOOC-CH2-COOH等五种单体,故A错误;
、HOOC-CH2-COOH等五种单体,故A错误;
B.互为同系物的是HOOC-COOH与HOOC-CH2-COOH;HO-CH2-CH2-OH与 ,对苯二甲酸和其他羧酸不是同系物,故B错误;
,对苯二甲酸和其他羧酸不是同系物,故B错误;
C.乙二醇催化氧化生成乙二醛,乙二醛催化氧化生成乙二酸,乙二酸即为草酸,故C正确;
D.高分子化合物为混合物,无固定熔沸点,1 mol上述链节完全水解需要氢氧化钠物质的量为 6mol,故D错误;
故选C.
点评 本题考查有机物的结构和性质,题目难度不大,注意根据高聚物判断有机物的单体为解答该题的关键,注意把握有机物的官能团的性质.

练习册系列答案
相关题目
17.有 X、Y 两种元素,原子序数≤20,X 的原子半径小于 Y,且 X、Y 原子的最外层电子数相同(选项中 m、n 均为正整数).下列说法正确的是( )
| A. | 若 HnXOm为强酸,则 X 的氢化物溶于水一定显酸性 | |
| B. | 若 X(OH)n为强碱,则 Y(OH)n 也一定为强碱 | |
| C. | 若 X 元素形成的单质是 X2,则 Y 元素形成的单质一定是 Y2 | |
| D. | 若 Y 的最高正价为+m,则 X 的最高正价一定为+m |
6.下表为元素周期表的一部分,参照元素①~⑧在表中的位置,请回答下列问题.
(1)画出⑤的离子结构示意图 .
.
(2)③、④、⑧的原子中半径最大的是④(写编号).
(3)④和⑥的最高价的氧化物的水化物中碱性强的是NaOH.②和⑦的气态氢化物中的稳定性强的是H2O(均填化学式).
(4)写出一种由①②组成且含有非极性键的物质的电子式 .
.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 .
.(2)③、④、⑧的原子中半径最大的是④(写编号).
(3)④和⑥的最高价的氧化物的水化物中碱性强的是NaOH.②和⑦的气态氢化物中的稳定性强的是H2O(均填化学式).
(4)写出一种由①②组成且含有非极性键的物质的电子式
 .
.
10.下列叙述中不正确的是( )
| A. | 电解时在电解池的阳极上不一定有阴离子放电 | |
| B. | 原电池跟电解池连接后,电子从原电池负极流向电解池阳极 | |
| C. | 电解池是将电能转化为化学能的装置 | |
| D. | 电解时,电源负极流出的电子数等于流入电源正极的电子数 |
7.下列关于油脂的叙述不正确的是( )
| A. | 天然油脂是混和物 | |
| B. | 油脂是天然高分子化合物 | |
| C. | 油脂在碱性溶液中能发生皂化反应 | |
| D. | 人造脂肪是液态的油催化加氢形成的 |
8.(1)一定条件下,CO2与1.0mol•L-1NaOH溶液充分反应放出的热量如表一:
表一:
该条件下CO2与NaOH溶液反应生成NaHCO3的热化学方程式为NaOH(aq)+CO2(g)═NaHCO3(aq)△H=-(4x-y)kJ/mol .
(2)用焦炭还原NO的反应为:2NO(g)+C(s)?N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒温容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如表二:
表二:
①甲容器中,0~40min内用NO的浓度变化表示的平均反应速率v(NO)=0.0125mol/(L•min).
②该反应的△Hb(填序号)
a.大于0 b.小于0 c.等于0d.不能确定
③丙容器达到平衡时,NO的转化率为60% .
(3)298K时,NH3•H2O的电离常数Kb=2×10-5,H2CO3的电离常数Kal=4×10-7,Ka2=4×10-11.在NH4HCO3溶液中,c(NH4+)>c(HCO3-)(填“>”、“<”或“=”);反应NH4++HCO3-+H2O?NH3•H2O+H2CO3的平衡常数K的数值(用科学计数法表示)为1.25×10-3.
表一:
| 反应序号 | CO2的物质的量/mol | NaOH溶液的体积/L | 放出的热量/KJ |
| 1 | 0.5 | 0.75 | x |
| 2 | 1.0 | 2.00 | y |
(2)用焦炭还原NO的反应为:2NO(g)+C(s)?N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒温容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如表二:
表二:
| 温度 t/min | 0 | 40 | 80 | 120 | 160 |
| 甲(673K) | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| 乙(T) | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
| 丙(673K) | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
②该反应的△Hb(填序号)
a.大于0 b.小于0 c.等于0d.不能确定
③丙容器达到平衡时,NO的转化率为60% .
(3)298K时,NH3•H2O的电离常数Kb=2×10-5,H2CO3的电离常数Kal=4×10-7,Ka2=4×10-11.在NH4HCO3溶液中,c(NH4+)>c(HCO3-)(填“>”、“<”或“=”);反应NH4++HCO3-+H2O?NH3•H2O+H2CO3的平衡常数K的数值(用科学计数法表示)为1.25×10-3.
 ,A在一定条件下有如图所示的转化关系.
,A在一定条件下有如图所示的转化关系.
 ,写出所有符合下列要求的E的同分异构体的结构简式:
,写出所有符合下列要求的E的同分异构体的结构简式: 、
、 .
. .
. .
.