题目内容
下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)==CO2(g) △H1 C(s)+1/2O2(g)==CO(g) △H2
②S(s)+O2(g)==SO2(g) △H3 S(g)+O2(g)==SO2(g) △H4
③H2(g)+1/2O2(g)==H2O(l) △H5 2H2(g)+O2(g)==2H2O(l) △H6
④CaCO3(s)==CaO(s)+CO2(g) △H7 CaO(s)+H2O(l)==Ca(OH)2(s) △H8
A.① B.④ C.②③④ D.①②③
C
【解析】
试题分析::①C(s)+O2(g)=CO2(g)反应是放热反应,△H1<0;C(s)+1/2O2(g)=CO(g)反应是放热反应△H2<0,一氧化碳生成二氧化碳是放热反应;△H1<△H2,故①不符合;②由于气态硫的能量高于固态硫的能量,因此气体硫燃烧生成二氧化硫放热多,但放热越多,△H越小,即△H3>△H4 ,故②符合;③H2(g)+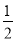 O2(g)=H2O(l) △H5<0,2H2(g)+O2(g)=2H2O(l)△H6<0,参加反应的氢气越多,放热越多,因此△H5>△H6 ,故③符合;③CaCO3(s)=CaO(s)+CO2(g)反应是吸热反应,△H7>0;CaO(s)+H2O(l)=Ca(OH)2(s),反应是放热反应,△H8<0;前者大于后者,△H7>△H8,故④符合,答案选C。
O2(g)=H2O(l) △H5<0,2H2(g)+O2(g)=2H2O(l)△H6<0,参加反应的氢气越多,放热越多,因此△H5>△H6 ,故③符合;③CaCO3(s)=CaO(s)+CO2(g)反应是吸热反应,△H7>0;CaO(s)+H2O(l)=Ca(OH)2(s),反应是放热反应,△H8<0;前者大于后者,△H7>△H8,故④符合,答案选C。
考点:考查反应热大小比较

练习册系列答案
相关题目
 3Zn(OH)2 + 2Fe(OH)3 + 4KOH。请写出该电池在充电时阴极的电极反应式: ;
3Zn(OH)2 + 2Fe(OH)3 + 4KOH。请写出该电池在充电时阴极的电极反应式: ;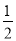 O2(g) ΔH=-485 kJ·mol-1
O2(g) ΔH=-485 kJ·mol-1 O2(g) ΔH=+485 kJ·mol-1
O2(g) ΔH=+485 kJ·mol-1
