题目内容
20.以下6种物质中选取序号填空(可重复选填).①二氧化碳 ②硫化氢 ③氯化铵 ④氢氧化钾 ⑤甲醛 ⑥乙醇
(1)含有非极性键的是⑥;
(2)含有配位键的是③;
(3)既含有σ键又含有π键的是①⑤;
(4)属于非极性分子的是①;
(5)分子的立体结构呈平面三角形的是⑤;
(6)属于离子晶体的是③④.
分析 (1)同种非金属元素之间形成非极性共价键;
(2)形成配位键两个原子,一方提供空轨道、一方提供孤对电子;
(3)既含有σ键又含有π键应为双键或三键;
(4)结构对称,正负电荷重心重叠的分子为非极性分子;
(5)分子的立体结构呈平面三角形的为sp2杂化;
(6)含有离子键的化合物为离子化合物,由离子化合物形成的晶体为离子晶体.
解答 解:(1)乙醇中含有C-C键,为非极性键,故答案为:⑥;
(2)氯化铵中含有配位键,故答案为:③;
(3)二氧化碳和甲醛中分别含有C=C键、C=O键,含有σ键又含有π键,故答案为:①⑤;
(4)二氧化碳为直线形分子,结构对称,为非极性分子,故答案为:①;
(5)甲醛中C为sp2杂化,且无孤电子对,为平面三角形,故答案为:⑤;
(6)氯化铵、氢氧化钾含有离子键,为离子化合物,形成的晶体为离子晶体,故答案为:③④.
点评 本题考查化学键及其分类,为高频考点,侧重于学生的分析能力的考查,明确元素的类别及元素的成键是解答本题的关键,难度较小.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
8.F、CI和Br都是第七主族元素,关于这三种元素原子的说法正确的是( )
| A. | 原子半径:F>CI>Br | B. | 最外层电子数都相同 | ||
| C. | 核外电子层数都相同 | D. | 最外层电子数都不相同 |
15.加热下列各物质没有单质生成的是( )
| A. | KMnO4 | B. | NH3•H2O | C. | HNO3 | D. | H2O2 |
12.已知R元素的原子有四个电子层,其最高价氧化物化学式R2O5,则R元素的名称为( )
| A. | 硫 | B. | 砷 | C. | 硒 | D. | 硅 |
9.下列实验中,反应速率加快是由催化剂引起的是( )
| A. | 把煤块变成煤粉燃烧更为剧烈 | |
| B. | 锌与稀硫酸反应制H2时加入少量CuSO4溶液而使反应速率加快 | |
| C. | 固态FeCl3和固态NaOH混合后,加入水能迅速产生沉淀 | |
| D. | 双氧水中加入少量MnO2,即可迅速放出气体 |
11.小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快.该小组通过实验探究其原因.请你和探究小组完成下列问题:
(1)提出合理假设.该实验中反应速率明显加快的原因可能是AC.
A.反应放热导致温度升高 B.压强增大
C.生成物的催化作用 D.反应物接触面积增大
(2)初步探究测定实验过程中不同时间溶液的温度,结果如表:
根据表中实验数据规律,结合实验假设你能得出的结论是温度不是反应速率明显加快的主要原因.
(3)进一步探究.查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用.为此,请你完成以下实验设计(将表格和实验目的补充完整):
表中X的值为,实验①和②探究Cu2+对实验的影响.
(1)提出合理假设.该实验中反应速率明显加快的原因可能是AC.
A.反应放热导致温度升高 B.压强增大
C.生成物的催化作用 D.反应物接触面积增大
(2)初步探究测定实验过程中不同时间溶液的温度,结果如表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
(3)进一步探究.查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用.为此,请你完成以下实验设计(将表格和实验目的补充完整):
| 实验 编号 | 铜片 质量/g | 0.1mol•L-1 硝酸/mL | 硝酸铜 溶液/mL | 亚硝酸钠 溶液/mL | 水的体积 /mL | 实验目的 |
| ① | 5 | 20 | 0 | 0 | 0.5 | 实验①和②探究Cu2+对实验的影响;实验①和③探究亚硝酸根的影响. |
| ② | 5 | 20 | 0.5 | 0 | 0 | |
| ③ | 5 | 20 | 0 | X | 0 |
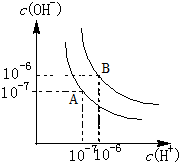 按要求填空:
按要求填空: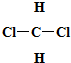 和
和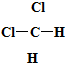 ⑥CH3CH2CH2CH3和
⑥CH3CH2CH2CH3和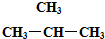
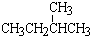 ;
; ③
③ .
.
 (R,R′,R″代表相同或不相同的烃基)
(R,R′,R″代表相同或不相同的烃基) .
. .
. .
.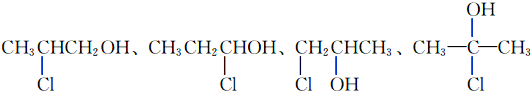 .
.