题目内容
7.将2L含有0.3mol CuSO4和0.4mol NaCl的水溶液用惰性电极电解一段时间后,在一个电极上得到0.3mol Cu后并析出2.24L(标准状况)气体,则另一电极上先后析出的气体的成分是什么?其物质的量分别为多少?分析 根据原子守恒得n(Cu)=n(CuSO4)=0.3mol,电解时阴极上Cu 2+先析出,然后H+放电生成H2,阴极生成n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,阴极转移电子物质的量=2(Cu)+2n(H2)=0.3mol×2+0.1mol×2=0.8mol,阳极上先Cl-放电,Cl-完全放电转移电子物质的量=0.4mol×1=0.4mol<0.8mol,则阳极上还生成O2,根据转移电子守恒计算生成氧气物质的量,据此分析解答.
解答 解:根据原子守恒得n(Cu)=n(CuSO4)=0.3mol,电解时阴极上Cu 2+先析出,然后H+放电生成H2,阴极生成n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,阴极转移电子物质的量=2(Cu)+2n(H2)=0.3mol×2+0.1mol×2=0.8mol,阳极上先Cl-放电,Cl-完全放电转移电子物质的量=0.4mol×1=0.4mol<0.8mol,则阳极上还生成O2,根据Cl原子守恒得n(Cl2)=$\frac{1}{2}$n(NaCl)=$\frac{1}{2}$×0.4mol=0.2mol,n(O2)=$\frac{0.8mol-0.4mol}{4}$=0.1mol,
答:另一电极上先后析出的气体的成分是Cl2和O2,其物质的量分别是0.2mol、0.1mol.
点评 本题以电解原理为载体考查物质的量有关计算,为高频考点,侧重考查学生分析计算能力,正确判断各个电极上发生的反应是解本题关键,阴阳极上转移电子守恒,根据转移电子守恒计算即可,题目难度不大.

练习册系列答案
相关题目
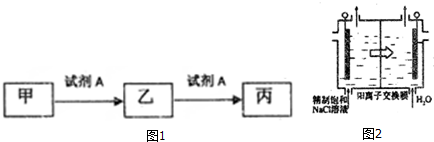
17.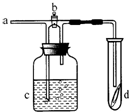 如图所示,从a处通入了氯气.若打开活塞b,d处的干燥有色布条不褪色,若关闭活塞b,d处的干燥有色布条褪色.下列判断正确的是( )
如图所示,从a处通入了氯气.若打开活塞b,d处的干燥有色布条不褪色,若关闭活塞b,d处的干燥有色布条褪色.下列判断正确的是( )
 如图所示,从a处通入了氯气.若打开活塞b,d处的干燥有色布条不褪色,若关闭活塞b,d处的干燥有色布条褪色.下列判断正确的是( )
如图所示,从a处通入了氯气.若打开活塞b,d处的干燥有色布条不褪色,若关闭活塞b,d处的干燥有色布条褪色.下列判断正确的是( )| A. | c中盛放的不可能是NaCl溶液 | B. | c中盛放的可能是浓硫酸 | ||
| C. | c中盛放的可能是足量NaOH溶液 | D. | a处通入的是干燥的氯气 |
18.下列反应过程中,同时有非极性共价键断裂和形成的是( )
| A. | 2H2+O2═H2O | B. | NH3+HCl═NH4Cl | ||
| C. | 4Fe(OH)2+2H2O+O2═4Fe(OH)3 | D. | 2Na2O2+2H2O═4NaOH+O2↑ |
15.下列物质既属于芳香烃,又属于苯的同系物的是( )
① ②
②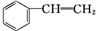 ③
③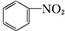 ④
④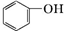 ⑤
⑤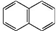
⑥
①
 ②
②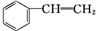 ③
③ ④
④ ⑤
⑤
⑥

| A. | ③④ | B. | ①⑥ | C. | ①②⑤⑥ | D. | ②⑤ |
2.下列说法不正确的是( )
| A. | 不能自发进行的氧化还原反应,通过电解的原理可以实现 | |
| B. | 电镀时保持电流恒定,升高温度不改变电解反应速率 | |
| C. | 电解精炼铜电解槽底部会形成含少量Ag、Fe、Pt等金属的阳极泥 | |
| D. | 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 | |
| E. | MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液,若电解电路中通过2mol电子,MnO2的理论产量为1mol | |
| F. | 燃料电池是将燃料燃烧所放出的能量转化为化学能的装置 |
12.由于金属锌本身的价值不高,在我国工业锌废料的回收利用率比较低,某课题组研究利用含少量铜、铁的粗锌制备硫酸锌及相关物质的资源综合利用,其工艺流程图(图中加入的物质均为足量)及有关数据如下:
请回答下列问题:
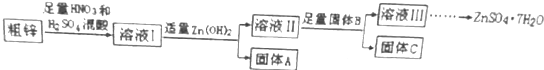
(1)固体A的主要成分是Fe(OH)3,加入固体B的主要作用是除去溶液Ⅱ中的Cu2+.
(2)粗锌中的铜与稀混酸溶液反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(3)若溶液Ⅱ中c(Cu2+)为0.05mol•L-1,则溶液Ⅱ的pH≤5.
(4)若B是Zn,取8.320gC完全溶解于500mL1mol•L-1稀硝酸中,共收集到2240mL气体,再向所得溶液中加入NaOH溶液至刚好生成沉淀最多,此时所得沉淀质量(m)的取值范围是13.42;若B是另一种物质,取部分C于试管中,加入盐酸后产生了有臭鸡蛋味气体,则该反应的离子方程式为ZnS+2H+=H2S↑+Zn2+.
请回答下列问题:

| 物质 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS |
| Ksp | 4.0×10-38 | 5.0×10-20 | 2.0×10-16 | 8.5×10-45 | 1.2×10-23 |
(2)粗锌中的铜与稀混酸溶液反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(3)若溶液Ⅱ中c(Cu2+)为0.05mol•L-1,则溶液Ⅱ的pH≤5.
(4)若B是Zn,取8.320gC完全溶解于500mL1mol•L-1稀硝酸中,共收集到2240mL气体,再向所得溶液中加入NaOH溶液至刚好生成沉淀最多,此时所得沉淀质量(m)的取值范围是13.42;若B是另一种物质,取部分C于试管中,加入盐酸后产生了有臭鸡蛋味气体,则该反应的离子方程式为ZnS+2H+=H2S↑+Zn2+.
19.下列性质能代表卤素通性的是( )
| A. | H2+X2═2HX | B. | X2+H20═HX+HXO | ||
| C. | NaX+AgNO3═AgX↓+NaNO3 | D. | 2NaX+H2SO4(浓)═Na2SO4+2HX |
17. 已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2
已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2
常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-和SO32-三种微粒的物质的量分数与溶液的关系如图所示,则下列说法中不正确的是( )
 已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2
已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-和SO32-三种微粒的物质的量分数与溶液的关系如图所示,则下列说法中不正确的是( )
| A. | 曲线3表示的微粒是SO32- | |
| B. | 溶液pH=4.2时,c(Na+)+c(H+)=c(OH-)+2c(SO32-) | |
| C. | 常温下,$\frac{{K}_{a1}}{{K}_{a2}}$=1000 | |
| D. | 溶液pH=1.2时:c(Na+)+c(H+)=c(OH-)+c(HSO3) |
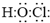 .二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠(NaClO3)和另一种氯的含氯酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-═ClO3-+ClO2-+H2O
.二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠(NaClO3)和另一种氯的含氯酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-═ClO3-+ClO2-+H2O