题目内容
15.锌-碳硫酸原电池(如图)工作时,下列叙述正确的是( )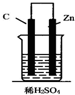
| A. | 正极反应为:Zn-2e-═Zn2+ | |
| B. | 电池反应式为:Zn+2H+═Zn2++H2↑ | |
| C. | 在闭合电路中,电子从碳极流向锌极 | |
| D. | 溶液中的H+移向锌极 |
分析 A、锌是负极,发生氧化反应;
B、电极反应是锌与氢离子发生氧化还原反应,电池反应式为:Zn+2H+═Zn2++H2↑;
C、原电池中,电子由负极沿导线流向正极;
D、原电池中阳离子向正极移动.
解答 解:A、锌是负极,发生氧化反应,电极反应式为:Zn-2e-═Zn2+,故A错误;
B、电极反应是锌与氢离子发生氧化还原反应,电池反应式为:Zn+2H+═Zn2++H2↑,故B正确;
C、原电池中,电子由负极沿导线流向正极,所以电子从锌极流向碳极,故C错误;
D、原电池中阳离子向正极移动,所以溶液中的H+移向碳极,故D错误;
故选B.
点评 本题考查原电池的工作原理,为高考常见题型,注意把握工作原理以及电极方程式的书写,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.运用元素周期律分析下面的推断,其中错误的是( )
| A. | 铍的氧化物的水化物可能具有两性 | |
| B. | 砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸 | |
| C. | 氢氧化铷[RbOH]易溶于水 | |
| D. | 硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
6.下列有关比较,顺序排列错误的是( )
| A. | 原子半径:Al>Mg>Na | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 熔点:纯铁>铝>铝合金 |
3.2011年是国际化学年,其主题为“化学--我们的生活 我们的未来”.恰值玛丽•居里夫人获得诺贝尔化学奖(发现了镭和钋元素)100周年.下列说法正确的是( )
| A. | 在日常生活中,倡导绿色化学,避免环境污染 | |
| B. | 镭在周期表中位于第ⅡA族,其放射性不会造成污染 | |
| C. | 钋在周期表中位于第ⅥA族,是金属性很强的金属 | |
| D. | 为了我们的生活,地下的煤和石油可大量开采 |
10.某有机物X能发生水解反应,水解产物为Y和Z.同温同压下,Y和Z的相对分子质量相同,化合物X可能是( )
| A. | 葡萄糖 | B. | 甲酸乙酯 | C. | 乙酸乙酯 | D. | 蔗糖(C12H22O11) |
20.下列物质中,可用来鉴别乙二醇、葡萄糖、乙酸的水溶液的一种试剂是( )
| A. | 金属钠 | B. | 溴水 | C. | 新制的氢氧化铜 | D. | 石蕊溶液 |
7.某有机化合物M的结构简式为 ,有关该化合物的叙述正确的是( )
,有关该化合物的叙述正确的是( )
 ,有关该化合物的叙述正确的是( )
,有关该化合物的叙述正确的是( )| A. | 该有机物属于芳香烃 | |
| B. | 该有机物不易溶于水 | |
| C. | 该有机物的原子一定处于同一平面 | |
| D. | 该有机物只能发生加成反应和酯化反应 |

 ;
; 和
和 ;
; .
.