题目内容
(8分)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2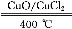 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,1 mol HCl被氧化,放出28.9 kJ的热量。
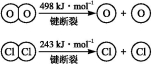
ⅱ.
(1)反应A的热化学方程式是 。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”) 。
(3)大气中的部分碘源于O3对海水中I-的氧化。O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g) IO-(aq)+O2(g) ΔH1
IO-(aq)+O2(g) ΔH1
②IO-(aq)+H+(aq)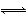 HIO(aq) ΔH2
HIO(aq) ΔH2
③HIO(aq)+I-(aq)+H+(aq)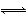 I2(aq)+H2O(l) ΔH3
I2(aq)+H2O(l) ΔH3
总反应的化学方程式为 ,其反应热ΔH= 。
(8分) (1)4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1 (2分)
2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1 (2分)
(2)32(1分) 强(1分)
(3)O3+2I-+2H+ I2+O2+H2O(2分) ΔH1+ΔH2+ΔH3(2分)
I2+O2+H2O(2分) ΔH1+ΔH2+ΔH3(2分)
【解析】
试题分析:(1)根据1 mol HCl被氧化,放出28.9 kJ的热量可以计算当有4摩尔氯化氢被氧化时放出的热量为28.9×4=115.6,所以根据热化学方程式的写法写热化学方程式为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1 ;(2)
2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1 ;(2)
考点: 反应热及热化学方程式书写

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
 c C(g)+d D(g),反应过程中,当其它条件不变时,C 的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
c C(g)+d D(g),反应过程中,当其它条件不变时,C 的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是 