题目内容
6.下列陈述I、II均正确并且有因果关系的是( )| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Fe2O3是红棕色粉末 | Fe2O3常用作红色涂料 |
| B | SiO2是两性氧化物 | SiO2可和HF反应 |
| C | Al2O3难溶于水 | Al2O3可用作耐火材料 |
| D | SO2有氧化性 | SO2可使溴水褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.依据氧化铁为红棕色粉末的物理性质解答;
B.两性氧化物与酸、碱反应产物都是盐和水;
C.耐火材料,应具有高的熔沸点;
D.二氧化硫具有还原性,能够被溴水氧化.
解答 解:A.氧化铁为红棕色粉末,可以用于红色涂料和油漆,陈述I、II均正确并且有因果关系,故A正确;
B.二氧化硅与氢氟酸反应生成四氟化硅和水,不是两性氧化物,陈述I错误,故B错误;
C.氧化铝可用作耐火材料,是因为氧化铝具有较高的熔沸点,与氧化铝不溶于水性质无关,故C错误;
D.SO2可使溴水褪色,体现二氧化硫的还原性,故D错误;
故选:A.
点评 本题考查了元素化合物知识,熟悉相关物质的化学性质是解题关键,注意审题:陈述I、II均正确并且有因果关系,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
16.含氯化镁、氯化钾、硫酸钠三种物质的混合液,已知其中氯离子有1.5mol,钾离子和钠离子共1.5mol,镁离子为0.5mol,则硫酸根离子的物质的量为( )
| A. | 0.1mol | B. | 0.5mol | C. | 0.15mol | D. | 0.25mol |
17.在水溶液中能大量共存的一组离子是( )
| A. | Fe3+、NH4+、HCO3-、SO42- | B. | H+、Fe2+、ClO-、Cl- | ||
| C. | Mg2+、Na+、SO42-、NO3- | D. | Al3+、Ag+、OH-、Br- |
11.下列有关材料的说法不正确的是( )
| A. | 制造普通水泥和玻璃的主要原料都用到石灰石 | |
| B. | 工业上制玻璃不会有温室气体的排放 | |
| C. | 玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料 | |
| D. | “中国”的英文单词叫China,这是由于中国制造的某种物质驰名世界,这种物质是陶瓷 |
15.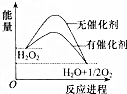 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+O2;△H=-Q1 kJ•mol-1 | |
| D. | 加入催化剂,减小了反应的热效应 |
16.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为2NA | |
| B. | 7 g CnH2n中含有的氢原子数目为NA | |
| C. | 任何气体单质在标况下体积若为22.4L,则含有2NA个原子 | |
| D. | 1mol Na2O2与水反应转移的电子数约为1.204×1024个 |
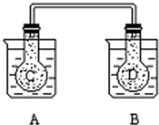 如图所示,25℃时,在烧杯A中装有50.00ml蒸馏水,烧杯B 中盛有50.00
如图所示,25℃时,在烧杯A中装有50.00ml蒸馏水,烧杯B 中盛有50.00