题目内容
某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O.已知H2S在反应中失去电子.回答下列问题:
(1)将氧化剂和还原剂及反应后生成的相应物质的化学式填入下面空格中(不需要配平):

(2)若反应过程中转移了0.3mol电子,则参加反应的HNO3的物质的量是 mol.
(1)将氧化剂和还原剂及反应后生成的相应物质的化学式填入下面空格中(不需要配平):

(2)若反应过程中转移了0.3mol电子,则参加反应的HNO3的物质的量是
考点:氧化还原反应,氧化还原反应的计算
专题:氧化还原反应专题
分析:(1)硝酸的氧化性大于硫,所以在该反应中硝酸作氧化剂,在反应中得电子化合价降低,则硫化氢在反应中失电子作还原剂,该反应方程式为:3H2S+2HNO3═3S+2NO+4H2O;
(2)反应中N元素化合价由+5价降低到+2价,结合元素化合价的变化计算.
(2)反应中N元素化合价由+5价降低到+2价,结合元素化合价的变化计算.
解答:
解:(1)硝酸的氧化性大于硫,所以在该反应中硝酸作氧化剂,在反应中得电子化合价降低,则硫化氢在反应中失电子作还原剂,该反应方程式为:3H2S+2HNO3═3S+2NO+4H2O,可表示为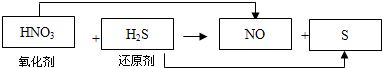 ,
,
故答案为: ;
;
(2)反应中N元素化合价由+5价降低到+2价,若反应过程中转移了0.3mol电子,则参加反应的HNO3的物质的量是
=0.1mol,
故答案为:0.1.
 ,
,故答案为:
 ;
;(2)反应中N元素化合价由+5价降低到+2价,若反应过程中转移了0.3mol电子,则参加反应的HNO3的物质的量是
| 0.3mol |
| 5-2 |
故答案为:0.1.
点评:本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握反应的特点,从元素化合价的角度认识氧化还原反应的相关概念、把握物质的性质,难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
| A、1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA |
| B、1mol/LK2SO4溶液所含K+数目为2NA |
| C、在标准状况下,22.4L水所含分子数目为NA |
| D、2.4gMg与足量盐酸完全反应时,失去电子数目为0.1NA |
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A、11.2L NO和11.2L 02混合后的分子总数为NA |
| B、1mol苯乙烯中含有的碳碳双键数为4NA |
| C、1 L 0.1mol?L-1Na2C03溶液中含有 0.1 NA个CO32- |
| D、1mol Cu与足量的稀HNO3反应,转移2 NA个电子 |
将15g CH4和C2H4的混合气体通入盛有足量溴水的容器中,溴水的质量增加了7g,则混合气体中CH4与C2H4的体积比为( )
| A、1:2 | B、2:1 |
| C、3:2 | D、2:3 |
wg铁粉和铝粉的混合物,和过量的NaOH反应,然后过滤,将沉淀完全收集放蒸发皿中加热到物质质量不再变化,称其质量与原混合物的质量相等.原混合物中铝粉的质量分数是( )
| A、25% | B、30% |
| C、55% | D、70% |
