题目内容
9.下列各组离子能大量共存的是( )| A. | Na+、Cu2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ | B. | H+、K+、HCO${\;}_{3}^{-}$、Ca2+ | ||
| C. | Ba2+、Mg2+、OH-、Cl- | D. | Fe3+、NH${\;}_{4}^{+}$、S2-、Cl- |
分析 A.四种离子之间不反应,能够共存;
B.氢离子与碳酸氢根离子反应;
C.镁离子与氢氧根离子反应生成难溶物氢氧化镁;
D.铁离子能够氧化硫离子.
解答 解:A.Na+、Cu2+、NO3-、SO42-之间不发生反应,能够大量共存,故A正确;
B.H+、HCO3-之间发生反应,在溶液中不能大量共存,故B错误;
C.Mg2+、OH-之间反应生成氢氧化钠沉淀,在溶液中不能大量共存,故C错误;
D.Fe3+、S2-之间发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
20.下列反应完成后没有沉淀的是( )
| A. | BaCl2溶液与Na2S03溶液加足量稀HNO3 | |
| B. | Ba(0H)2溶液与KN03溶液加足量稀H2SO4 | |
| C. | AgN03溶液与Na2C03溶液加足量稀盐酸 | |
| D. | Ca(0H)2溶液与FeCl3溶液加足量稀HNO3 |
4.下列反应的离子方程式正确的是( )
| A. | 向亚磷酸溶液中加入过量的烧碱溶液(亚磷酸是二元弱酸):H3PO3+3OH-═PO33-+3H2O | |
| B. | 2mol•L-1的AlCl3溶液和7mol•L-1的NaOH溶液等体积混合:2Al3++7OH-═Al(OH)3↓+AlO${\;}_{2}^{-}$+2H2O | |
| C. | 用硝酸酸化的硝酸铁溶液可以刻蚀银饰:Fe3++Ag═Fe2++Ag+ | |
| D. | H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH-+18O2 |

 C6H14
C6H14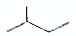 C5H12
C5H12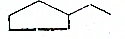 C7H14
C7H14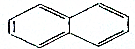 C10H8.
C10H8.