题目内容
已知:(1)H2(g)+O2(g)═H2O(g)△H1=a kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(g)△H2=b kJ?mol-1
(3)H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1
(4)2H2(g)+O2(g)═2H2O(l)△H4=d kJ?mol-1
下列关系式中正确的是 ( )
(2)2H2(g)+O2(g)═2H2O(g)△H2=b kJ?mol-1
(3)H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1
(4)2H2(g)+O2(g)═2H2O(l)△H4=d kJ?mol-1
下列关系式中正确的是 ( )
| A、a<c<0 |
| B、b>d>0 |
| C、2a=b<0 |
| D、2c=d>0. |
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:依据热化学方程式书写原则分析,反应系数变化,焓变随之变化,反应方向变化,焓变要变化符号;
焓变小于零的反应是放热的,大于零的反应是吸热的,据此分析解答.
焓变小于零的反应是放热的,大于零的反应是吸热的,据此分析解答.
解答:
解:热化学方程式中化学计量数只表示物质的量,
(1)H2(g)+O2(g)═H2O(g)△H1=a kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(g)△H2=b kJ?mol-1
(3)H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1
(4)2H2(g)+O2(g)═2H2O(l)△H4=d kJ?mol-1
水从气态变为液态,放热,所以(1)与(3)比较,(3)放出的热量多,焓变小于零的反应是放热的,所以0>a>c,(2)与(4)比较,(4)放出的热量多,所以0>b>d,
热化学方程式反应系数变化,焓变随之变化,所以b=2a<0,d=2c<0,
故选C.
(1)H2(g)+O2(g)═H2O(g)△H1=a kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(g)△H2=b kJ?mol-1
(3)H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1
(4)2H2(g)+O2(g)═2H2O(l)△H4=d kJ?mol-1
水从气态变为液态,放热,所以(1)与(3)比较,(3)放出的热量多,焓变小于零的反应是放热的,所以0>a>c,(2)与(4)比较,(4)放出的热量多,所以0>b>d,
热化学方程式反应系数变化,焓变随之变化,所以b=2a<0,d=2c<0,
故选C.
点评:本题考查热化学反应方程式,比较反应热及热量时注意正负号,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
由乙炔(C2H2)、苯和乙醛组成的混和物中,测得含碳元素的质量百分含量为72%,则混和物中氧元素的质量百分含量为( )
| A、19.56% | B、20% |
| C、22% | D、25% |
以Al2(SO4)3溶液为原料之一,在实验室里制取少量Al(OH)3,并且易于分离,最好向溶液中加入( )
| A、NaOH 溶液 |
| B、氢氧化钡溶液 |
| C、氨水溶液 |
| D、澄清石灰水 |
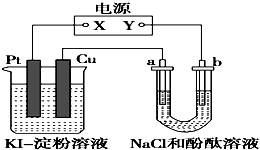 CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )| A、若a极变红,则在Pt电极上:2I--2e-═I2,淀粉遇碘变蓝 |
| B、若b极变红,则在Pt电极上:4OH--4e-═2H2O+O2↑,O2将I-氧化为I2,淀粉遇碘变蓝 |
| C、若a极变红,则在Cu电极上:2Cu+4I--4e-═2CuI↓+I2,碘遇淀粉变蓝 |
| D、若b极变红,则在Cu极上:Cu-2e-═Cu2+,Cu2+显蓝色 |
在2A(g)+3B(g)=C(g)+4D(g)的反应中,下列表示该反应的化学反应速度最快的是( )
| A、v (A)=0.5 mol/(L?s) |
| B、v (B)=0.9 mol/(L?s) |
| C、v (C)=0.8 mol/(L?s) |
| D、v (D)=1.0 mol/(L?s) |
已知下列两个反应中:4P(白磷,s)+5O2(g)=2P2O5(s)△H=-Q1 KJ/mol4P(红磷,s)+5O2(g)=2P2O5(s)△H=-Q2 KJ/mol且Q1>Q2,则( )
| A、燃烧白磷放出的能量比燃烧红磷放出的能量多 |
| B、白磷转化为红磷是属于放热反应 |
| C、白磷和红磷互为同素异形体 |
| D、等质量的白磷和红磷,白磷含有的能量比红磷的低 |
下列说法正确的是( )
| A、其他条件不变,增大某一反应物浓度,反应物的转化率一定都增大 |
| B、对于有气体参加的反应,其他条件不变增大压强,体积缩小,体系中各气体的浓度一定增大 |
| C、对于有气体参加的反应,改变压强使平衡向右移动,生成的气体的浓度一定增大 |
| D、增大反应物的浓度,平衡向右移动,生成物的体积分数一定增大 |
下列说法正确的是( )
| A、工业用电解熔融AlCl3的方法制金属铝 |
| B、铅蓄电池工作时,正极反应为:PbO2+2e-+4H++SO42-=PbSO4+2H2O |
| C、电解饱和食盐水时,用铁作阳极,Cl- 发生氧化反应 |
| D、电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |