题目内容
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、125g CuSO4?5H2O晶体中含有Cu2+离子数小于0.5NA |
| B、7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA |
| C、由S4、S6、S8组成的硫蒸气6.4 g,其中所含硫原子数一定为0.2NA |
| D、3.6 gC与3.36LO2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
考点:阿伏加德罗常数
专题:
分析:A、依据离子晶体的特点分析即可;
B、硫化钠和过氧化钠的摩尔质量相等,1mol过氧化钠中含有1mol阴离子;
C、都是单质,则硫原子的物质的量为
mol;
D、依据气体摩尔体积的条件应用分析.
B、硫化钠和过氧化钠的摩尔质量相等,1mol过氧化钠中含有1mol阴离子;
C、都是单质,则硫原子的物质的量为
| m |
| 32 |
D、依据气体摩尔体积的条件应用分析.
解答:
解:A、CuSO4?5H2O为离子晶体,在晶体中不存在铜离子,存在的是晶胞结构单元,故A错误;
B、1mol过氧化钠中含有1mol阴离子,7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA,故B错误;
C、S2、S6和S8的混合物中只有S原子,则硫原子的物质的量为
=0.2mol,则所含硫原子数一定为0.2NA,故C正确;
D、由于温度和压强不知,无法计算气体的物质的量,只有标准状况下生成CO分子数为0.3NA,故D错误;故选C.
B、1mol过氧化钠中含有1mol阴离子,7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA,故B错误;
C、S2、S6和S8的混合物中只有S原子,则硫原子的物质的量为
| 6.4 |
| 32 |
D、由于温度和压强不知,无法计算气体的物质的量,只有标准状况下生成CO分子数为0.3NA,故D错误;故选C.
点评:本题考查阿伏伽德罗常数的计算,考查知识点全面,题量过大,难度不大.

练习册系列答案
相关题目
下列实验设计或实验操作中,正确的是( )
A、 |
B、 |
C、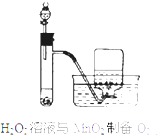 |
D、 |
1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和8体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
| A、乙烯 | B、丙烯 | C、丁烯 | D、丁二烯 |
下列说法或表示方法正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、由C(金刚石,s)═C(石墨,s)△H=-1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=285.8 kJ?mol-1 |
| D、稀溶液中H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
下列关于甲、乙、丙、丁四种仪器装置的有关用法中不合理的是( )


| A、甲装置:可用来证明硫的非金属性比硅强 |
| B、乙装置:橡皮管的作用是能使水顺利流下 |
| C、丙装置:用图示的方法能检查此装置的气密性 |
| D、丁装置:可在瓶中先装满水,气体由②口入,收集NO气体 |
下列说法正确的是( )
| A、盐桥在电化学中可导通左右半池,其作用和用铜导线连接完全一致 |
| B、室温时,酸碱中和滴定的终点刚好是pH=7的点 |
| C、pH计和广泛pH试纸的精确度一致,只是pH计使用更方便 |
| D、0.1 mol?L-1的醋酸中加入水或加入冰醋酸均可使醋酸电离平衡向电离方向移动 |
高温下CuFeS2的反应之一为2CuFeS2+7O2
CuSO4 +CuO+Fe2O3 +3SO2,下列该反应的叙述正确的是( )
| ||
| A、CuFeS2中硫的化合价为+1 |
| B、CuFeS2发生还原反应 |
| C、1mol CuFeS2完全反应转移13mol电子 |
| D、CuSO4和SO2既是氧化产物,又是还原产物 |
下列有关说法正确的是( )
| A、纯碱溶液加水稀释,溶液中所有离子浓度均减小 |
| B、镀锡铁制品镀层受损后,铁制品比受损前更易被腐蚀 |
| C、将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| D、合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动 |

