题目内容
15.已知OCN-中C显+4价,在反应OCN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)中,如果有6mol Cl2完全反应,则被氧化的OCN-的物质的量是( )| A. | 2 mol | B. | 3 mol | C. | 6mol | D. | 4 mol |
分析 OCN-中碳为+4价,推测N是-3价,反应中N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,根据电子转移数目守恒计算被氧化的OCN-的物质的量.
解答 解:OCN-中碳为+4价,推测N是-3价,反应中N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,
令被氧化的OCN-的物质的量为n mol,据电子转移数目守恒有:
6mol×2=n mol×[0-(-3)],解得n=4,
故选D.
点评 本题考查氧化还原反应的有关计算,难度不大,确定N元素化合价是关键,注意理解氧化还原反应中电子转移守恒的运用.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
20.硅被誉为无机非金属材料的主角.有科学家提出硅是“21世纪的能源”“未来的石油”.下列有关说法正确的是( )
| A. | 硅的含量居第二位,在地球上有丰富的单质硅资源,如石英、水晶的主要成分都是SiO2 | |
| B. | 单质硅是一种良好的半导体材料,可用于制造太阳能电池 | |
| C. | 存放NaOH溶液的试剂瓶应用玻璃塞 | |
| D. | 60gSiO2含有1NA个SiO2分子 |
3.一定温度下,在1L密闭容器中,反应N2+3H2?2NH3达到化学平衡状态的标志是( )
| A. | N2:H2:NH3=1:3:2 | |
| B. | N2、H2、NH3的物质的量不再改变 | |
| C. | 混合气体的密度保持不变 | |
| D. | 单位时间里每增加1mol N2,同时增加3mol H2 |
10.下列化学用语正确的是( )
| A. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 次氯酸的结构式:H-O-Cl | |
| C. | S2-的结构示意图: | |
| D. | CO2的比例模型: |
20.下列实验正确的是( )
| A. |  蒸发、浓缩 | B. | 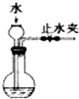 检查装置气密性 | ||
| C. | 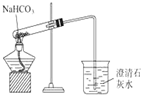 碳酸氢钠受热分解 | D. | 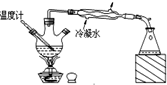 分离沸点不同且互溶的液体混合体 |
7.海洋约占地球表面的71%,具有十分巨大的开发潜力,目前的南海争端威胁到我们国家的核心利益.下列关于海水资源的说法中,错误的是( )
| A. | 海带中含有碘元素 | |
| B. | 海水中含有大量氯元素 | |
| C. | 蒸馏法是海水淡化的主要方法之一 | |
| D. | 开发海水资源可以不考虑是否对环境有污染 |
4.下列说法正确的是( )
| A. | 分子式为C9H10且含有碳碳双键的芳香烃有5种 | |
| B. | 结构为…-CH═CH-CH═CH-CH═CH-…的高分子化合物,其单体是乙烯 | |
| C. | 三分子甲醛合成三聚甲醛( )的反应属于加成反应 )的反应属于加成反应 | |
| D. | 丙烯酸(CH2═CHCOOH)和山梨酸(CH3CH═CHCH═CHCOOH)不是同系物,它们与氢气充分反应后的产物也不是同系物 |
5.可判断某溶液呈中性的依据是( )
| A. | 溶液的c(H+)=10-7 mol/L | B. | 溶液的溶质为盐 | ||
| C. | 溶液中既含有H+又含有OH- | D. | 混合溶液中,pH=-$\frac{lg{K}_{w}}{2}$ |