题目内容
要使溶液中存在大量的K+、Na+、H+、NO3-和SO42-五种离子,则在蒸馏水中至少溶解几种物质( )
| A、2种 | B、3种 | C、4种 | D、5种 |
考点:电解质在水溶液中的电离
专题:
分析:由于溶液中含K+、Na+、H+、NO3-和SO42-五种离子,又要求至少溶解几种物质,因此溶液中一种物质至少含三种离子,即酸式盐或者碱式盐.
解答:
解:由于溶液中含K+、Na+、H+、NO3-和SO42-五种离子,又要求至少溶解几种物质,因此溶液中一种物质至少含三种离子,由题意知这种物质应该是含氢离子的酸式盐,所以应该是KHSO4、NaNO3或者KNO3、NaHSO4;
故选A.
故选A.
点评:本题考查强弱电解质在水溶液中的存在形式,学生容易忽略硫酸氢盐,在水溶液中完全电离.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式为( )
| A、大理石溶于盐酸中:CO32-+2H+=CO2↑+H2O |
| B、氯化铝加到过量氢氧化钠溶液中:Al3++4OH-=[Al(OH)4]- |
| C、(NH4)2CO3溶液中加入过量Ba(OH)2溶液:NH4++OH-=NH3↑+H2O |
| D、氯化铁溶液中加入铜片:Fe3++Cu=Fe2++Cu2+ |
下列有关化学键的叙述,正确的是( )
| A、离子化合物中不一定含有离子键 |
| B、单质分子中均不存在化学键 |
| C、由C元素形成的单质不一定是原子晶体 |
| D、含有共价键的化合物一定是共价化合物 |
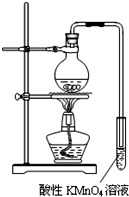 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.