题目内容
下列各物质中,按熔点由低到高排列正确的是
[ ]
A. 、
、 、Hg
、Hg
 、
、 、Hg
、HgB.铝硅合金、铝、硅
C.Na、K、Rb
D.SiC、NaCl、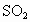
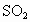
答案:B
解析:
解析:
|
思路分析:构成晶体的微粒间的相互作用越强,熔点就越高.一般原子晶体熔点最高,离子晶体熔点较高,分子晶体熔点较低,金属晶体由于不同金属中金属键强度差别较大,其熔点高低差别较大. A中Hg呈液态,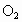 、 、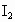 分别呈气、固态,熔点 分别呈气、固态,熔点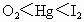 ;B中合金的熔点较其成分金属Al低,硅为原子晶体,熔点高,符合题意;C中同主族的Na、K、Rb金属键依次减弱,熔点降低;D中SiC为原子晶体,NaCl为离子晶体, ;B中合金的熔点较其成分金属Al低,硅为原子晶体,熔点高,符合题意;C中同主族的Na、K、Rb金属键依次减弱,熔点降低;D中SiC为原子晶体,NaCl为离子晶体,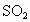 为分子晶体,熔点降低. 为分子晶体,熔点降低.
指点迷津:各类晶体熔点比较,一般有原子晶体>离子晶体>分子晶体;但也有例外,要注意具体情况具体分析.金属晶体由于金属键差别较大,故其熔点范围变化较大.同种晶体间微粒间的作用力越强,熔点就越高. |

练习册系列答案
 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
下列各物质中,按熔点由高到低的顺序排列的是( )
| A.H2Te > H2Se > H2S > H2O | B.KCl>NaCl>LiCl>HCl |
| C.Sr>Ba>Ca>Be | D.金刚石>SiC>晶体硅 |