题目内容
1.下列电离方程式正确的是( )| A. | CaCl2═Ca2++Cl2 | B. | H2SO4═2 H++SO42- | ||
| C. | Ba(OH)2═Ba++2OH- | D. | NaHCO3═Na++H++CO32- |
分析 A.氯化钙为强电解质,在溶液中完全电离出钙离子和2个氯离子,不会电离出氯气;
B.硫酸为强电解质,在溶液中完全电离出氢离子和硫酸根离子;
C.钡离子的表示方法错误,钡离子应该带有2个单位正电荷;
D.碳酸氢钠为强电解质,在溶液中完全电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开.
解答 解:A.氯化钙在溶液中完全电离出钙离子和氯离子,正确的电离方程式为:CaCl2═Ca2++2Cl-,故A错误;
B.硫酸在溶液中完全电离,其电离方程式为:H2SO4═2H++SO42-,故B正确;
C.氢氧化钡为强电解质,在溶液中完全电离,其正确的电离方程式为:Ba(OH)2═Ba++2OH-,故C错误;
D.碳酸氢根离子需要保留整体形式,碳酸氢钠正确的电离方程式为:NaHCO3═Na++HCO3-,故D错误;
故选B.
点评 本题考查了电离方程式的书写,题目难度不大,正确判断强弱电解质为解答关键,注意掌握电离方程式的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
12.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.5 g甲基(-CH3)所含电子数目为NA | |
| B. | 0.1 mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA | |
| C. | 由2H和18O所组成的水11 g,其中所含的中子数为5NA | |
| D. | 1 mol Fe溶于过量硝酸,电子转移数为2NA |
9.关于1mol•L-1的硫酸溶液的下列叙述中,不正确的是( )
| A. | 1 L该溶液中含溶质98 g | |
| B. | 从10 mL该溶液中取出5 mL后,剩余溶液的浓度不变 | |
| C. | 将4.9 g浓硫酸加入盛有50 mL蒸馏水的烧杯中充分溶解就可配得该浓度的硫酸溶液 | |
| D. | 该浓度的硫酸具有酸的通性 |
16.如图所示各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为( )
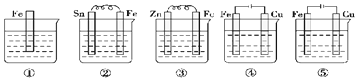

| A. | ⑤②①③④ | B. | ③②⑤④① | C. | ⑤④③②① | D. | ⑤②①④③ |
6.下列说法正确的是( )
①铁在潮湿空气中生锈是自发过程
②NH4HCO3受热分解是熵增的过程
③反应焓变是决定反应能否自发进行的唯一因素
④自发过程中,熵值都是增大的
⑤温度、压强一定时,放热且熵增加的反应一定能自发进行.
①铁在潮湿空气中生锈是自发过程
②NH4HCO3受热分解是熵增的过程
③反应焓变是决定反应能否自发进行的唯一因素
④自发过程中,熵值都是增大的
⑤温度、压强一定时,放热且熵增加的反应一定能自发进行.
| A. | ①②③④⑤ | B. | ①②⑤ | C. | ③④ | D. | ④⑤ |
13.对可逆应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 化学反应速率关系是:2υ正(NH3)=3υ正(H2O) | |
| B. | 达到化学平衡时,4υ正(O2)=5υ逆(NO) | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
10.配制一定物质的量浓度溶液时,会导致所配溶液浓度偏大的操作是( )
| A. | 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中 | |
| B. | 用量筒量取浓硫酸时,俯视刻度线 | |
| C. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 | |
| D. | 定容时俯视刻度线 |
 ,它的共价键属于极性(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为
,它的共价键属于极性(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为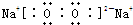 ;含有极性共价键和非极性共价键的化合物的电子式为
;含有极性共价键和非极性共价键的化合物的电子式为 .
. .
. A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的$\frac{3}{4}$倍;C与E同主族.
A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的$\frac{3}{4}$倍;C与E同主族.