题目内容
7.下列离子方程式的书写中正确的是( )| A. | 等体积、等浓度的KHSO4溶液与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 在次氯酸中加入碳酸钠:2HClO+CO32-═2ClO-+H2O+CO2↑ | |
| C. | 钾与水反应:2K+2H2O═2K++2OH-+H2↑ | |
| D. | 氯化钠溶液中通入氟气:F2+2Cl-═2F-+Cl2↑ |
分析 A.等体积、等浓度的KHSO4溶液与Ba(OH)2溶液反应生成硫酸钡、氢氧化钠和水;
B.不符合反应客观事实;
C.二者反应生成氢氧化钾和氢气;
D.不符合反应客观事实,氟气通入氯化钠溶液与水反应生成氢氟酸和氧气.
解答 解:A.等体积、等浓度的KHSO4溶液与Ba(OH)2溶液反应,离子方程式:Ba2++OH-+H++SO42-═BaSO4↓+H2O
,故A错误;
B.在次氯酸中加入碳酸钠生成次氯酸钠和碳酸氢钠,离子方程式:HClO+CO32-═ClO-+HCO3-,故B错误;
C.钾与水反应,离子方程式:2K+2H2O═2K++2OH-+H2↑,故C正确;
D.氯化钠溶液中通入氟气,离子方程式:2F2+2H2O═4HF+O2↑,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循原子个数守恒规律,题目难度不大.

练习册系列答案
相关题目
17.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5 mol1,3-丁二烯分子中含有C=C双键数为NA | |
| D. | 标准状况下,11.2 L己烷所含分子数为0.5 NA |
15.25℃时,某一元弱酸HA的电离平衡常数为Ka,A?的水解平衡常数为Kh,该温度下向20mL 0.lmol•L-1 HA溶液中逐滴加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略反应导致的温度变化).下列说法不正确的是( )

| A. | 滴定过程中总是存在:Ka>Kh | |
| B. | 点②所示溶液中存在:c(Na+)=c(A-) | |
| C. | 点③所示溶液中存在:c(Na+)=c(A-)+c(HA) | |
| D. | 向点①所示溶液中加水:$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$比值减小 |
2.关于Na+和Na的性质叙述正确的是( )
| A. | 都具有金属光泽 | B. | 都是强还原剂 | ||
| C. | 焰色反应现象相同 | D. | 电子层结构相同 |
19.填写溴、碘在不同溶剂中的颜色
| 水 | CCl4 | 汽油(苯) | |
| Cl2 | 黄绿色 | 黄绿色 | 黄绿色 |
| Br2 | 橙红色 | ||
| I2 | 紫红色 |
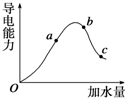 在25℃时,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
在25℃时,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
 2Fe(s)+3CO2(g) △H= kJ/mol。
2Fe(s)+3CO2(g) △H= kJ/mol。 e2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡。
e2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡。