题目内容
18.下列说法正确的( )| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 离子化合物中只能含离子键 | |
| D. | 只有非金属原子间才能形成共价键 |
分析 A.含有共价键的化合物可能是离子化合物,也可能是共价化合物;
B.只含共价键的化合物是共价化合物;
C.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键;
D.全部由非金属元素组成的化合物可能是离子化合物,可能是共价化合物.
解答 解:A.含有共价键的化合物可能是离子化合物,也可能是共价化合物,如NaOH是离子化合物、HCl是共价化合物,故A错误;
B.只含共价键的化合物是共价化合物,所以共价化合物中一定含有共价键,故B正确;
C.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,如过氧化钠等,故C错误;
D.全部由非金属元素组成的化合物可能是离子化合物,可能是共价化合物,如铵盐是离子化合物、硝酸是共价化合物,故D错误;
故选B.
点评 本题考查化学键和化合物的关系,侧重考查基本概念,把握物质的构成微粒及化学键的形成条件即可解答,注意离子键和共价键的区别,易错选项是D.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
13.在恒温恒容密闭容器中发生反应NH2COONH4(s)?2NH3(g)+CO2(g),不能判断该反应已达到化学平衡的是( )
| A. | 2v(NH3)=v(CO2) | |
| B. | 密闭容器中总压强不变 | |
| C. | 密闭容器中混合气体的密度不变 | |
| D. | 密闭容器中混合气体的平均摩尔质量不变 |
14.下列说法正确的是( )
| A. | 0.1 mol•L-1的醋酸加水稀释,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
13.已知:pOH=-lgc(OH-),298K时,向20.00mL0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH和pOH与加入盐酸体积关系如图所示.下列说法正确的是( )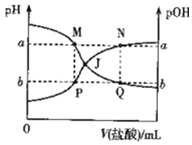

| A. | 曲线PJN表示溶液中pH的变化 | |
| B. | M点水的电离程度比Q点大 | |
| C. | M、P两点的数值之和a+b=14 | |
| D. | pH与pOH交叉点J对应的V(盐酸)=20.00 mL |
3.下列有关叙述中正确的是( )
| A. | 在提纯鸡蛋中的蛋白质时,可向鸡蛋清溶液中加入浓硝酸,然后将所得沉淀滤出,即得较纯的蛋白质 | |
| B. | 可用过滤的方法除去四氯化碳中的I2 | |
| C. | 苯和溴苯的混合物可用分液漏斗分液分离 | |
| D. | 乙酸乙酯中混有乙酸,可用饱和Na2CO3溶液洗涤,然后分液分离出乙酸乙酯 |
10.有机化学在日常生活应用广泛,下列有关说法不正确的是( )
| A. | 相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大 | |
| B. | 煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 | |
| C. | 甲苯和Cl2光照下的反应与乙醇和乙酸反应属于同一类型的反应 | |
| D. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
7.下列说法正确的是( )
| A. | 干冰升华时须吸收大量的热,这就是化学反应中的吸热现象 | |
| B. | 酒精常被用作酒精灯和内燃机的燃料,说明酒精燃烧是放热反应 | |
| C. | 木炭常温下不燃烧,加热才能燃烧,说明木炭燃烧是吸热反应 | |
| D. | 酸碱中和反应都放热,因此可以将其设计成原电池,将化学能转换成电能供人们使用 |
8.化学与生产、生活、社会密切相关,下列说法错误的是( )
| A. | 中国古代利用明矾溶液淸除铜镜表面的铜锈,是利用了明矾的酸性 | |
| B. | 碘是人体内必须的微量元素,所以富含高碘酸钾的食物适合所有人群 | |
| C. | “光化学烟雾”“臭氧空洞”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 用加入足量氢氧化钠溶液共热的方法可以区分地沟油与矿物油 |
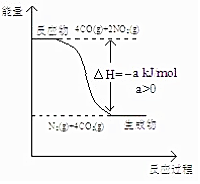 研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.
研究 NOx、SO2、CO 等大气污染气体的处理具有重要意义.