题目内容
1.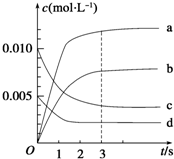 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(2)图中表示NO2的变化的曲线是b,
(3)用O2的浓度变化表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是ac
a.将容器体积变为1Lb.适当升高温度c.增大O2的浓度d.选择高效的催化剂.
分析 (1)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变;
(2)根据表格知,随着反应的进行,一氧化氮的物质的量减小,则平衡向正反应方向移动,二氧化氮的物质的量逐渐增大,根据一氧化氮和二氧化氮之间转化关系式计算平衡时二氧化氮的物质的量,从而确定曲线;
(3)先计算一氧化氮的反应速率,再根据同一化学反应中同一时间段内,各物质的反应速率之比等于其计量数之比计算氧气的反应速率;
(4)为使该反应的反应速率增大,可采用增大压强、升高温度、加入催化剂、增大反应物浓度等方法,再结合平衡移动原理分析解答.
解答 解:(1)a、当v (NO2)=2v (O2)时,该反应不一定达到平衡状态,故a错误;
b、该反应是一个反应气体气体体积改变的可逆反应,当达到平衡状态时,各物质的浓度不变,则容器内压强保持不变,故b正确;
c、v逆(NO):v正(O2)=2:1时,该反应达到平衡状态,所以当v逆(NO)=2v正(O2),该反应达到平衡状态,故c正确;
d、根据质量守恒定律知,混合物质量始终不变,容器的体积不变,则容器内混合气体的密度始终不变,所以不能据此判断是否达到平衡状态,故d错误;
故答案为:bc;
(2)根据表格知,随着反应的进行,一氧化氮的物质的量减小,则平衡向正反应方向移动,二氧化氮的物质的量逐渐增大,当反应达到平衡状态时,参加反应的n(NO)=(0.020-0.007)mol=0.013mol,根据二氧化氮和一氧化氮的关系式知,平衡状态时生成n(NO2)等于参加反应的n(NO),所以为0.013mol,c(NO2)=$\frac{0.013mol}{2L}$,故选b,
故答案为:b;
(3)0~2s时,v(NO)=$\frac{\frac{0.02mol-0.008mol}{2L}}{2s}$=0.003mol/(L.s),同一化学反应中同一时间段内,各物质的反应速率之比等于其计量数之比,
所以v(O2)=$\frac{1}{2}$v(NO)=0.0015mol•L-1•s-1,
故答案为:0.0015mol•L-1•s-1;
(4)a.将容器体积变为1L,体积缩小相当于增大容器中的压强,压强增大,反应速率增大,平衡正向进行,故a正确;
b.适当升高温度,反应速率增大但平衡向逆反应方向移动,故b错误;
c.增大O2的浓度反应速率增大,且该反应向正反应方向移动,故c正确;
d.选择高效催化剂能增大反应速率,但平衡不移动,故d错误;
故答案为:a c.
点评 本题考查了化学平衡状态的判断、化学反应速率的计算等知识点,根据v=$\frac{△c}{△t}$、v(正)=v(逆)来分析解答即可,题目难度不大.

 星级口算天天练系列答案
星级口算天天练系列答案| A. | C3H7Cl | B. | C3H8 | C. | CH2Cl2 | D. | C2H6O |
| A. | 治理拥堵,减少汽车尾气排放,大力发展清洁能源可以有效减少雾霾 | |
| B. | 铜的金属活动性比铝弱,可以用铜罐代替铝罐储运浓硝酸 | |
| C. | 光化学烟雾的形成和氮的氧化物有关,硫的氧化物是形成硫酸型酸雨的主要物质 | |
| D. | 硫化钠和亚硫酸钠的固体如果长期暴露在空气中容易变质 |
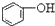 >HCO3-,下列化学方程式正确的是( )
>HCO3-,下列化学方程式正确的是( )| A. | 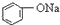 +H2O+CO2→ +H2O+CO2→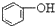 +Na2CO3 +Na2CO3 | B. | 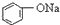 +NaHCO3→ +NaHCO3→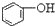 +Na2CO3 +Na2CO3 | ||
| C. | 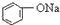 +H2O+CO2→ +H2O+CO2→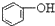 +NaHCO3 +NaHCO3 | D. | 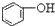 +NaHCO3→ +NaHCO3→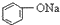 +H2O+CO2 +H2O+CO2 |
| A. | Br2和HBrO3均是氧化产物 | |
| B. | BrF3既是氧化剂,又是还原剂 | |
| C. | BrF3的氧化性强于O2 | |
| D. | 反应中,若生成1molBr2,则反应转移6NA个电子 |
| 发展阶段 | 原子结构模型 | 重要科学家 |
| 1 | 近代原子论 | |
| 2 | 汤姆生 | |
| 3 | 原子行星模型 |
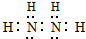 .
. HCO3-+OH-. 0.2mol/L该溶液中离子浓度由大到小的顺序为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
HCO3-+OH-. 0.2mol/L该溶液中离子浓度由大到小的顺序为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).