题目内容
3.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | Cl2 | CO2 | CaCl2 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl |
| A. | ②③④ | B. | ②③④⑤ | C. | ①③④ | D. | ①③④⑤ |
分析 ①石灰水过量,有CaCO3和CaSO3沉淀生成;
②氯气与氯化钙溶液中水反应不会产生沉淀,二氧化碳与氯化钙溶液不反应;
③硝酸根在酸性环境下能够氧化二氧化硫生成硫酸根离子;
④二氧化氮与水反应生成硝酸,硝酸能够氧化二氧化硫生成硫酸根离子;
⑤当NH3不足时,最终无沉淀生成.
解答 解:①由于石灰水过量,因此必有CaCO3和CaSO3沉淀生成,故正确;
②氯气与氯化钙溶液中水反应不会产生沉淀,二氧化碳与氯化钙溶液不反应,故错误;
③硝酸根在酸性环境下能够氧化二氧化硫生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀,故正确;
④二氧化氮与水反应生成硝酸,硝酸能够氧化二氧化硫生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀,故正确;
⑤当NH3过量时溶液中CaCO3沉淀生成,发生反应的化学方程式为:2NH3+CO2+CaCl2+H2O═CaCO3 ↓+2NH4C1;当NH3不足时,最终无沉淀生成,发生反应的化学方程式为:2NH3+2CO2+CaCl2+2H2O═Ca(HCO3)2+2NH4C1,故错误;
故选:C.
点评 本题考查元素化合物知识,准确把握相关物质的性质是解题关键,注意反应物用量对反应的影响,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列有关实验现象的描述中,正确的是( )
| A. | 氢气在氯气中燃烧,产生大量白烟 | |
| B. | 钠在空气中燃烧,最终得到白色固体 | |
| C. | 向硅酸钠溶液中滴加稀盐酸,产生白色胶状物 | |
| D. | 向氯化铝溶液中滴加氨水,先产生白色沉淀,后沉淀消失 |
3.下列说法正确的是( )
| A. | 配制Na2S溶液时,为了抑制S2-的水解,常加入少量氢氧化钠 | |
| B. | 明矾用于净水过程只发生物理变化 | |
| C. | 把纯水加热水的电离程度增大,但水仍然是中性的,pH=7 | |
| D. | 加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体 |
8.下列电子式中,正确的是( )
| A. | 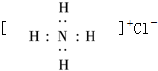 | B. | 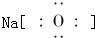 | ||
| C. | 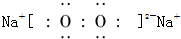 | D. | 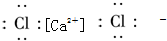 |
15.在常温下,下列溶液中有关微粒浓度的关系正确的是( )
| A. | 0.1mol•L-1(NH4)2Fe(SO4)2溶液:c (SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| B. | 0.1mol•L-1pH为4的NaHSO3溶液中:c(HSO3-)>c(H2SO3)>c(SO32-) | |
| C. | 0.1 mol•L-1 Na2S溶液中:2c(Na+)═c(S2-)+c(HS-)+c(H2S) | |
| D. | 某二元弱酸的酸式盐NaHA溶液:c(Na+)+c(H+)═c(OH-)+c(HA-)+c(A2-) |
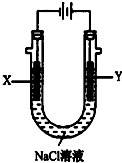
12.在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3.现将碳跟浓硫酸共热产生的气体X和碳跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )

| A. | 洗气瓶中产生的沉淀是碳酸钡 | |
| B. | 洗气瓶中产生的沉淀是硫酸钡 | |
| C. | 在Z导管出来的气体中无二氧化碳 | |
| D. | 反应一段时间后洗气瓶中溶液的酸性减弱 |
 甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.