题目内容
1.要证明某溶液中不含有Fe3+而可能含有Fe2+,进行如下操作时最佳顺序( )①加入足量氯水
②加入足量KMnO4溶液
③加入少量NH4SCN溶液.
| A. | ①③ | B. | ③② | C. | ③① | D. | ②③ |
分析 先根据Fe3+的特征反应判断溶液不含Fe3+;然后加入氧化剂,如果含有Fe2+,Fe2+被氧化剂氧化成Fe3+溶液变成红色,以此证明Fe2+的存在.
解答 解:因为KSCN与Fe3+作用使溶液显红色,与Fe2+作用无此现象,可以先滴加NH4SCN溶液,不显红色,说明原溶液不含有Fe3+,
再滴加氯水后显红色,说明滴加氯水后溶液中有Fe3+,证明原溶液含有Fe2+,即操作顺序为③①,
故选C.
点评 本题考查常见离子的检验,为高频考点,把握发生的氧化还原反应、试剂的先后顺序为解答的关键,侧重分析与应用能力的考查,注意离子检验的特征试剂,题目难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
11.下列各组物质的燃烧热相等的是( )
| A. | 碳和一氧化碳 | B. | 1mol 碳和2mol 碳 | ||
| C. | 1mol 乙炔和2mol 碳 | D. | 淀粉和纤维素 |
12.查处酒后驾驶采用的“便携式测量仪”是以燃料电池为工作原理,在酸性环境中,乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-=X+2H+.下列说法中正确的是( )
| A. | 燃料电池属于一次电池 | |
| B. | 另一极的电极反应式为:O2+4e-+2H2O=4OH- | |
| C. | 乙醇在正极发生氧化反应 | |
| D. | 电池总反应为:2CH3CH2OH+O22CH3CHO+2H2O |
16.下列关于强电解质和弱电解质的下列叙述中正确的是( )
| A. | 强电解质和弱电解质的本质区别在于:强电解质易溶于水,弱电解质 难溶于水 | |
| B. | 强电解质都是可溶性化合物,弱电解质都是难溶性化合物 | |
| C. | 强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子 | |
| D. | 强电解质溶液的导电能力强,弱电解质溶液的导电能力弱 |
6.下列基团:-CH3、-OH、-COOH、-C6H5,相互两两组成的有机物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
10.下列各项叙述中正确的是( )
| A. | 电子层序数越大,s原子轨道的形状相同,半径越大 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,释放能量,由基态转化成激发态 | |
| D. | 杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 |
11.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-=Cu(OH)2↓CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+=CO2↑+H2OBaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-=CaCO3↓Ca(NO3)2+Na2CO3═CaCO3↓+NaNO3 | |
| D. | H++OH-=H2OBa(OH)2+H2SO4═BaSO4↓+2H2O |
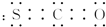 ,其分子呈直线形.
,其分子呈直线形. .
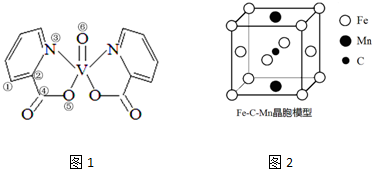
.
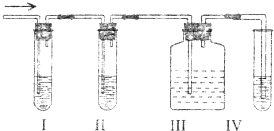 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:
在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题: