题目内容
13.按要求完成下列内容.(1)写出下列物质的电离方程式
盐酸HCl=H++Cl-
氢氧化钠溶液NaOH=Na++OH-
氯化钡溶液BaCl2=Ba2++2Cl-
碳酸氢钠溶液NaHCO3=Na++HCO3-
(2)写出下列反应的离子方程式
①锌和稀硫酸溶液的反应:Zn+2H+=Zn2++H2↑
②碳酸钙与稀盐酸的反应:CaCO3+2H+=Ca2++CO2↑+H2O
③氯化铜溶液与氢氧化钠溶液的反应:Cu2++2OH-=Cu(OH)2↓
(3)写出符合离子方程式Ag++Cl-=AgCl↓的一种化学方程式AgNO3+HCl=AgCl↓+HNO3.
分析 (1)电离方程式是用化学式和离子符号表示电离过程的式子,强酸、强碱、绝大部分盐是强电解质,全部电离,用“=”表示;弱酸、弱碱、水是弱电解质,部分电离,用“?”表示;
(2)①锌和稀硫酸反应生成硫酸锌和氢气;
②碳酸钙与稀盐酸反应生成二氧化碳、水和氯化钙;
③氯化铜与氢氧化钠反应生成氢氧化铜和氯化钠;
(3)离子方程式Ag++Cl-=AgCl↓,表示硝酸银与可溶性盐酸盐或者盐酸反应.
解答 解:(1)盐酸是强酸,全部电离,电离方程式为HCl=H++Cl-,氢氧化钠是强碱,全部电离,电离方程式为NaOH=Na++OH-,氯化钡是盐,电离方程式为BaCl2=Ba2++2Cl-,碳酸氢钠是盐,电离方程式为NaHCO3=Na++HCO3-,碳酸氢根是弱酸的酸式酸根,部分电离:HCO3-?H++CO32-,
故答案为:HCl=H++Cl-;NaOH=Na++OH-;BaCl2=Ba2++2Cl-;NaHCO3=Na++HCO3-;
(2)①锌和稀硫酸反应生成硫酸锌和氢气,实质是锌和氢离子的反应,离子方程式为Zn+2H+=Zn2++H2↑,故答案为:Zn+2H+=Zn2++H2↑;
②碳酸钙与稀盐酸反应生成二氧化碳、水和氯化钙,离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
③氯化铜与氢氧化钠反应生成氢氧化铜和氯化钠,实质是铜离子与氢氧根的反应:Cu2++2OH-=Cu(OH)2↓,故答案为:Cu2++2OH-=Cu(OH)2↓;
(3)离子方程式Ag++Cl-=AgCl↓可以表示硝酸银与盐酸反应,化学方程式为:AgNO3+HCl=AgCl↓+HNO3,
故答案为:AgNO3+HCl=AgCl↓+HNO3.
点评 本题考查了电离方程式、离子方程式的书写,题目难度不大,明确反应的实质是将解题关键,注意电荷守恒、原子个数守恒.

| A. | 碱金属都可以保存在煤油中 | |
| B. | 碱金属在空气中燃烧都能生成M2O(M表示碱金属) | |
| C. | 随着原子序数的增加,碱金属的熔点降低 | |
| D. | 碱金属着火应用泡沫灭火剂更好 |
| A. | 水与冰 | B. | O2与O3 | C. | 丁烷和正丁烷 | D. | 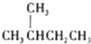 与 与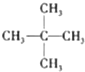 |
 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
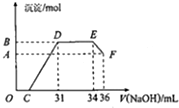
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示.
请回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O.
(2)B与A的差值为0.008mol,B点对应的沉淀的物质的量为0.032mol,C点对应的氢氧化钠溶液的体积为7ml.
| A. | 分散质粒子直径在1~100nm之间 | B. | 可用丁达尔效应区别这两种物质 | ||
| C. | 能用过滤的方法将它们分离 | D. | 都呈红褐色 |
| A. | 单质硅常用作半导体材料 | |
| B. | 硅酸钠是制备木材防火剂的原料 | |
| C. | 二氧化硅是制备光导纤维的基本原料 | |
| D. | 硅酸可由二氧化硅与水直接反应制得 |
①CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
则CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)的△H为( )
| A. | +478.7kJ•mol-1 | B. | -764.5 kJ•mol-1 | ||
| C. | -478.7kJ•mol-1 | D. | +764.5kJ•mol-1 |
| A. | 正丁烷和异丁烷的一氯取代物都只有两种,它们的沸点也相同 | |
| B. | 乙烯分子与苯分子都能与H2发生加成反应,说明二者均含碳碳双键 | |
| C. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 | |
| D. | 乙醛加入Cu(OH)2粉末并加热可看到红色沉淀生成 |