题目内容
在同温同压下,下列各组热化学方程式中△H1>△H2的是( )
| A、2H2(g)+O2(g)═2H2O(l);△H1 2H2(g)+O2(g)═2H2O(g);△H2 | ||||
| B、S(g)+O2(g)═2SO2(g);△H1 S(s)+O2(g)═2SO2(g);△H2 | ||||
C、C(s)+
| ||||
D、H2(g)+Cl2(g)═2HCl(g);△H1
|
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:A、液态水变为气态水的过程是吸热过程;
B、固体硫变为气态硫需要吸收热量;
C、碳单质完全燃烧放热多于不完全燃烧放的热.
D、化学反应方程式的系数加倍,焓变数值加倍.
B、固体硫变为气态硫需要吸收热量;
C、碳单质完全燃烧放热多于不完全燃烧放的热.
D、化学反应方程式的系数加倍,焓变数值加倍.
解答:
解:A、物质的燃烧反应是放热的,所以焓变是负值,液态水变为气态水的过程是吸热的,故△H1<△H2,故A错误;
B、物质的燃烧反应是放热的,所以焓变是负值,固体硫变为气态硫需要吸收热量,所以△H1>△H2,故B错误;
C、碳单质完全燃烧生成二氧化碳放热多于不完全燃烧生成一氧化碳放的热,反应的焓变是负值,故△H1>△H2,故C错误;
D、化学反应方程式的系数加倍,焓变数值加倍,该化合反应是放热的,所以焓变值是负值,2△H1=△H2,△H1<△H2,故D正确;
故选D.
B、物质的燃烧反应是放热的,所以焓变是负值,固体硫变为气态硫需要吸收热量,所以△H1>△H2,故B错误;
C、碳单质完全燃烧生成二氧化碳放热多于不完全燃烧生成一氧化碳放的热,反应的焓变是负值,故△H1>△H2,故C错误;
D、化学反应方程式的系数加倍,焓变数值加倍,该化合反应是放热的,所以焓变值是负值,2△H1=△H2,△H1<△H2,故D正确;
故选D.
点评:本题考查了物质反应能量变化分析判断,主要是盖斯定律的应用,物质量不同、状态不同、产物不同,反应的能量变化本题,题目较简单.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列关于有机化合物的说法不正确的是( )
| A、乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
| B、乙酸可与NaHCO3溶液反应生成CO2 |
| C、蛋白质和油脂在一定条件下都能水解 |
| D、葡萄糖和麦芽糖互为同系物 |
浓硝酸不具有的性质是( )
| A、吸水性 | B、酸性 |
| C、强氧化性 | D、易挥发性 |
下列说法正确的是( )
| A、K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 |
| B、NaCl、Na2CO3、NaOH三者饱和溶液的pH逐渐变大 |
| C、NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低 |
| D、金、银、铜金属活动性顺序逐渐减弱 |
在反应2SO2(g)+O2(g)═2SO3(g) 中,下列情况能够降低该反应速率的是( )
| A、升高温度 |
| B、减小压强 |
| C、使用催化剂 |
| D、增大SO2的浓度 |
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )

| A、甲池中,b电极是负极 |
| B、a电极的电极反应式C2H5OH+16OH--12e-═2CO32-+11H2O |
| C、一段时间后,用湿润淀粉KI试纸靠近乙池d电极变蓝放电 |
| D、乙池在反应前后溶液的pH不变充电 |
下列反应属于吸热反应的是( )
| A、镁与稀盐酸反应 |
| B、CO燃烧生成CO2 |
| C、生石灰溶于水 |
| D、氢氧化钙与氯化铵晶体混合 |
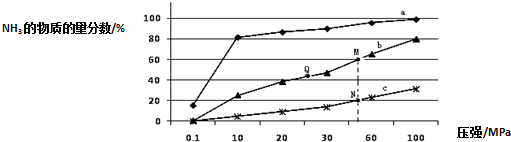

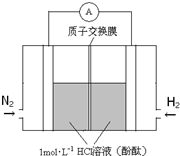 研究氮的固定具有重要意义.
研究氮的固定具有重要意义.