题目内容
某Mn+核外有a个电子,该元素的某种原子的质量数为A,则该原子的核内中子数为( )
| A、A-a+n |
| B、A-a-n |
| C、A+a-n |
| D、A+a+n |
考点:质子数、中子数、核外电子数及其相互联系
专题:
分析:在阳离子中,质子数=核外电子数+电荷数,中子数=质量数-质子数.
解答:
解:Mn+离子有a个电子,电荷数为n,则质子数=核外电子数+电荷数=a+n,故中子数=质量数-质子数=A-(a+n)=A-a-n,
故选:B.
故选:B.
点评:本题考查核外电子数、质子数、中子数、质量数、电荷数之间的关系,难度不大.要注意在阳离子中,质子数=核外电子数+电荷数.

练习册系列答案
相关题目
用R代表短周期元素,R原子最外层的p能级上的未成对电子只有2个.下列关于R的描述中正确的是( )
| A、R的氧化物一定能溶于水 |
| B、R的最高价氧化物所对应的水化物一定是H2RO3 |
| C、R的氧化物一定能与NaOH溶液反应 |
| D、R是非金属元素 |
根据元素所在元素周期表中位置,判断下列元素都能做为半导体材料的是( )
| A、Si、K | B、C、Al |
| C、Si、Ge | D、As、Se |
下列化学用语表示正确的是( )
A、H2O、Na2O的电子式都可用 表示 表示 |
B、Cl、Br、I的+1价含氧酸的结构式都可用“ ”表示 ”表示 |
| C、乙酸、乙酸乙酯、葡萄糖的分子式都可用“CnH2nOn”表示 |
| D、碳酸、亚硫酸的电离方程式都可用“H2XO3?2H++XO32-”表示 |
 如图所示,烧杯中试管内有一枚铁钉,放置数天后观察:
如图所示,烧杯中试管内有一枚铁钉,放置数天后观察:
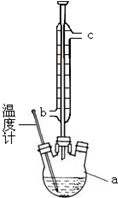 阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为: