题目内容
6. 按要求回答下列问题:
按要求回答下列问题:(1)向CH3COOH水溶液中加入水,平衡CH3COOH?H++CH3COO-将向正反应方向(填“正反应方向”、“逆反应方向”或“不”)移动,达新平衡状态时,溶液中c(CH3COO-)与原平衡时相比减小(填“增大”、“减小”或“不变”),溶液中c(OH-) 与原平衡时相比增大(填“增大”、“减小”或“不变”).
(2)K通常表示化学平衡常数,对于反应Cl2+H2O?H++Cl-+HClO其化学平衡常数K的表达式为:K=$\frac{c({H}^{+})•c(C{l}^{-})•c(HClO)}{c(C{l}_{2})}$.
(3)下列说法中正确的是
A.pH=1和pH=2的盐酸,c(H+)之比为1:2
B.某溶液中存在的离子只有Cl-、OH-、NH4+、H+,该溶液中离子浓度大小关系不可能为c(Cl-)>c(H+)>c(NH4+)>c(OH-)
C.0.1mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c (H2CO3)
D.升高温度,弱电解质的电离常数一定增大
E.某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的曲线如图所示.Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b.
分析 (1)加水稀释促进酸的电离;溶液中醋酸根离子浓度减小,氢离子浓度减小,根据Kw判断氢氧根离子浓度;
(2)平衡常数为生成物离子(或分子)浓度系数次幂之积除以反应物离子(或分子)浓度系数次幂之积反应;
(3)A.pH是氢离子浓度的负对数;
B.溶液为HCl和NH4Cl的混合溶液时,可能存在c(Cl-)>c(H+)>c(NH4+)>c(OH-);
C.HCO3-的水解程度大于电离程度;
D.升高温度促进弱电解质的电离;
E.醋酸为弱酸,存在电离平衡,当加水稀释时,氢离子浓度减小较慢,以此判断醋酸稀释时,pH的变化曲线.
解答 解:(1)加水稀释促进酸的电离;溶液中醋酸根离子浓度减小,氢离子浓度减小,根据Kw判断氢氧根离子浓度;
(2)平衡常数为生成物离子(或分子)浓度系数次幂之积除以反应物离子(或分子)浓度系数次幂之积反应,则反应Cl2+H2O?H++Clˉ+HClO其化学平衡常数K的表达式为:K=$\frac{c({H}^{+})•c(C{l}^{-})•c(HClO)}{c(C{l}_{2})}$;
故答案为:K=$\frac{c({H}^{+})•c(C{l}^{-})•c(HClO)}{c(C{l}_{2})}$;
(3)A.pH=1和pH=2的盐酸,氢离子浓度分别为0.1mol/L,0.01mol/L,则氢离子浓度之比1:10,故A错误;
B.溶液为等物质的量的HCl和NH4Cl的混合溶液时,铵根离子水解,浓度减小,所以c(H+)>c(NH4+),则离子浓度大小关系可能存在c(Cl-)>c(H+)>c(NH4+)>c(OH-),故B错误;
C.HCO3-的水解程度大于电离程度,电离生成CO32-,水解生成H2CO3,所以c (H2CO3)>c(CO32-),则0.1mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c (H2CO3)>c(CO32-),故C错误;
D.升高温度促进弱电解质的电离,则电离常数增大,故D正确;
E.相同温度下,pH相等的醋酸和盐酸中,二者c(H+)相等,加水稀释过程中,醋酸电离出H+导致醋酸溶液中c(H+)大于盐酸,所以稀释过程中醋酸pH小于盐酸,则Ⅱ为醋酸稀释时pH的变化曲线,酸抑制水电离,酸中氢离子浓度越大其抑制水电离程度越大,所以水电离程度:a<b,故E正确;
故答案为:DE.
点评 本题考查弱电解质的电离、离子浓度大小比较、电离平衡常数等知识点,明确溶液中溶质及影响电离平衡的因素是解本题关键,侧重考查学生分析能力,题目难度中等.

| A. | 10g CO和10g N2 | B. | 10g C2H4和10g C3H6 | ||
| C. | 5.6L O2(标准状况)和0.5mol H2O | D. | 224mL He(标准状况)和1.6g CH4 |
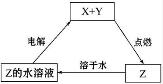
| A. | Z可能是氯化钠 | B. | Z可能是三氧化硫 | C. | X可能是金属铜 | D. | Y不可能是氢气 |
| A. | 能发生银镜反应 | |
| B. | 遇碘水不显兰色 | |
| C. | 与新制Cu(OH)2悬浊液反应,生成红色沉淀 | |
| D. | 有甜味 |
| A. | 纯碱-Na2CO3 | B. | 熟石灰-Ca(OH)2 | ||
| C. | 明矾-Al2(SO4)3•12H2O | D. | 胆矾-CuSO4•5H2O |
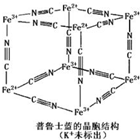 普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )| A. | 化学式可以表示为KFe2(CN)6 | |
| B. | 每一个立方体中平均含有24个π键 | |
| C. | 普鲁士蓝不属于配位化合物 | |
| D. | 每个Fe3+周围与之相邻的Fe2+离子有12个 |
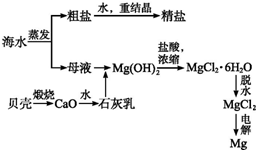 海水的综合利用可以制备金属镁,其流程如图所示:
海水的综合利用可以制备金属镁,其流程如图所示: