题目内容
 原子序数依次增大的四种短周期元素X、Y、Z、W,其相关信息如下表:
原子序数依次增大的四种短周期元素X、Y、Z、W,其相关信息如下表:| 元素 | 相关信息 |
| X | X的一种同素异形体是一种最软的矿物,常用于制造电极 |
| Y | Y的氢化物常温下呈气态,其水溶液能使酚酞试液变红 |
| Z | Z的最高价氧化物的水化物,在熔化状态下电离出离子数和电荷数均相等的阴阳离子 |
| W | W的基态原子的每个原子轨道均有电子填充,但只有一个未成对电子 |
(2)X、Y形成的气态氢化物中,易溶于水的是
(3)层状晶体g-X3Y4(用X3Y4表示),渗有少量金属或非金属后,常用于光催化分解水.水热法合成g-X3Y4是将W3X3Y3和ZY3在惰性气体中,在180℃反应12小时,再经洗涤除去食盐而制得.其化学方程式:
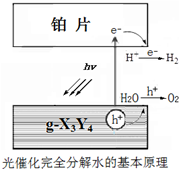
(4)g-X3Y4做催化剂,完全光分解水过程的基本原理,如图所示:
阳极反应过程为:
g-X3Y4+2hv→g-X3Y4+2h++2e
2H2O+2h+→2H2O+→2?OH+2H+
2?OH→H2O+
| 1 |
| 2O2 |
式中hv 表示光子,h+表示电子激发迁移后的空穴,有强氧化性;?OH表示羟基自由基.请写出阴极反应式:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X的一种同素异形体是一种最软的矿物,常用于制造电极,且X为短周期元素,则X为C元素;
Y的氢化物常温下呈气态,其水溶液能使酚酞试液变红,Y的氢化物的水溶液呈碱性,则Y为N元素;
Z的最高价氧化物的水化物,在熔化状态下电离出离子数和电荷数均相等的阴阳离子,且Z为短周期元素,其原子序数大于Y,则Z为Na元素;
W的基态原子的每个原子轨道均有电子填充,但只有一个未成对电子,且W原子序数大于Z,为短周期元素,则W为Cl元素,再结合物质结构、性质分析解答.
Y的氢化物常温下呈气态,其水溶液能使酚酞试液变红,Y的氢化物的水溶液呈碱性,则Y为N元素;
Z的最高价氧化物的水化物,在熔化状态下电离出离子数和电荷数均相等的阴阳离子,且Z为短周期元素,其原子序数大于Y,则Z为Na元素;
W的基态原子的每个原子轨道均有电子填充,但只有一个未成对电子,且W原子序数大于Z,为短周期元素,则W为Cl元素,再结合物质结构、性质分析解答.
解答:
解:X的一种同素异形体是一种最软的矿物,常用于制造电极,且X为短周期元素,则X为C元素;
Y的氢化物常温下呈气态,其水溶液能使酚酞试液变红,Y的氢化物的水溶液呈碱性,则Y为N元素;
Z的最高价氧化物的水化物,在熔化状态下电离出离子数和电荷数均相等的阴阳离子,且Z为短周期元素,其原子序数大于Y,则Z为Na元素;
W的基态原子的每个原子轨道均有电子填充,但只有一个未成对电子,且W原子序数大于Z,为短周期元素,则W为Cl元素,
(1)W为Cl元素,其原子核外有3个电子层、最外层有7个电子,则W位于第三周期第VIIA族,元素的非金属性越强,其最高价氧化物的水化物酸性越强,酸性:硝酸>碳酸,所以非金属性N>C,
故答案为:三;ⅦA;硝酸比碳酸强;
(2)X是C元素、Y是N元素,X、Y形成的气态氢化物中,易溶于水的是NH3,因为氨气和水都是极性分子,根据相似相溶原理、氨气和水分子之间易形成氢键知,氨气极易溶于水;Y的氢化物是氨气、Z的氢化物是NaH,氨气属于分子晶体、NaH属于离子晶体,离子晶体熔点高于分子晶体,所以Y和Z的氢化物熔点较高的是NaH,故答案为:NH3;NaH;
(3)水热法合成g-C3N4是将Cl3C3N3和NaN3在惰性气体中,在180℃反应12小时,再经洗涤除去食盐而制得,同时该反应还生成氮气,则反应方程式为3NaN3+Cl3C3N3
C3N4+3NaCl+4N2↑,故答案为:3NaN3+Cl3C3N3
C3N4+3NaCl+4N2↑;
(4)光催化分解水是半导体材料C3N4在特定波长的光照下,电子激发形成空穴,电子转入导带,在导带和禁带形成带隙,带隙比分解水产生氢气和氧气的电位差要大很多,能实现电解水.导带中电子迁移到(通常是Pt等)表面,发生反应2H++2e-=H2↑;空穴迁移到禁带半导体表面,发生反应过程如题给所示,完成电解水的过程;电解质通常选用全氟磺酸膜作为质子交换介质,也可以用玻璃纤维强化的磷酸碳纤维介质.由于禁带的电位高,可以利用其氧化废水中还原性成分,降低污水COD等用途.由于过程中是利用光电池电解水,故而能量转化形式为:光能→电能→化学能,考虑到学生实际,所以答案可以简化为:光能→化学能,故答案为:2H++2e-=H2↑;光能→(电能→)化学能.
Y的氢化物常温下呈气态,其水溶液能使酚酞试液变红,Y的氢化物的水溶液呈碱性,则Y为N元素;
Z的最高价氧化物的水化物,在熔化状态下电离出离子数和电荷数均相等的阴阳离子,且Z为短周期元素,其原子序数大于Y,则Z为Na元素;
W的基态原子的每个原子轨道均有电子填充,但只有一个未成对电子,且W原子序数大于Z,为短周期元素,则W为Cl元素,
(1)W为Cl元素,其原子核外有3个电子层、最外层有7个电子,则W位于第三周期第VIIA族,元素的非金属性越强,其最高价氧化物的水化物酸性越强,酸性:硝酸>碳酸,所以非金属性N>C,
故答案为:三;ⅦA;硝酸比碳酸强;
(2)X是C元素、Y是N元素,X、Y形成的气态氢化物中,易溶于水的是NH3,因为氨气和水都是极性分子,根据相似相溶原理、氨气和水分子之间易形成氢键知,氨气极易溶于水;Y的氢化物是氨气、Z的氢化物是NaH,氨气属于分子晶体、NaH属于离子晶体,离子晶体熔点高于分子晶体,所以Y和Z的氢化物熔点较高的是NaH,故答案为:NH3;NaH;
(3)水热法合成g-C3N4是将Cl3C3N3和NaN3在惰性气体中,在180℃反应12小时,再经洗涤除去食盐而制得,同时该反应还生成氮气,则反应方程式为3NaN3+Cl3C3N3
| ||
| 惰性气体 |
| ||
| 惰性气体 |
(4)光催化分解水是半导体材料C3N4在特定波长的光照下,电子激发形成空穴,电子转入导带,在导带和禁带形成带隙,带隙比分解水产生氢气和氧气的电位差要大很多,能实现电解水.导带中电子迁移到(通常是Pt等)表面,发生反应2H++2e-=H2↑;空穴迁移到禁带半导体表面,发生反应过程如题给所示,完成电解水的过程;电解质通常选用全氟磺酸膜作为质子交换介质,也可以用玻璃纤维强化的磷酸碳纤维介质.由于禁带的电位高,可以利用其氧化废水中还原性成分,降低污水COD等用途.由于过程中是利用光电池电解水,故而能量转化形式为:光能→电能→化学能,考虑到学生实际,所以答案可以简化为:光能→化学能,故答案为:2H++2e-=H2↑;光能→(电能→)化学能.
点评:以物质结构为基础,考查原子结构、分子结构,元素周期表和元素周期律,化学方程式的书写,电极反应式的书写,不同形式能量间的相互转化,理解电化学反应原理,难点是(4)题.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
常温下,下列各溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1 mol?L-1的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| B、将pH=6的H2SO4稀释1000倍后,c(H+)=2 c(SO42-) |
| C、浓度分别为0.1 mol?L-1和0.01 mol?L-1的CH3COOH溶液中:c(CH3COO-)前者是后者的10倍 |
| D、浓度均为0.1 mol?L-1的NaCN溶液和CH3COONa溶液中,c(CN-)<c(CH3COO-) |
下列各物质在一定条件下发生反应不能产生氧气的是( )
| A、过氧化钠遇水 |
| B、过氧化钠遇二氧化碳 |
| C、次氯酸见光分解 |
| D、钠放入硫酸铜溶液 |
下列各澄清溶液中分别通入过量的CO2,能观察到有沉淀或浑浊出现的是( )
①硅酸钠 ②苯酚 ③苯酚钠 ④石灰水 ⑤漂白粉 ⑥偏铝酸钠.
①硅酸钠 ②苯酚 ③苯酚钠 ④石灰水 ⑤漂白粉 ⑥偏铝酸钠.
| A、①③④⑤ | B、②⑤⑥ |
| C、②③④⑤⑥ | D、①③⑥ |
对于反应A(g)+3B(g)=2C(g)+2D(g),下列数据表示反应进行得最快的是( )
| A、v(A)=1.4mol/(L?s) |
| B、v(B)=3.6mol/(L?s) |
| C、v(C)=2mol/(L?s) |
| D、v(D)=3.2mol/(L?min) |
下列说法正确的是( )
| A、所有自发进行的化学反应都是放热反应 |
| B、自发进行的化学反应,一定是△H<0,△S>0的反应 |
| C、熵增且放热的反应一定是自发反应 |
| D、熵值增大的反应都能自发进行 |
 ,写出生成A的化学方程式:
,写出生成A的化学方程式: