题目内容
1840年,盖斯根据一系列实验事实得出规律:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同.”这是有关反应热的重要规律--盖斯定律.已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:C(s,金刚石)+O2(g)═CO2(g)△H=-395.4kJ/mol,C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ/mol,则金刚石转化为石墨时的热化学方程式为: 由此看来更稳定的碳的同素异形体为 .若取金刚石和石墨的混合晶体共1mol在O2中完全燃烧,产生的热量为Q kJ,则金刚石和石墨的物质的量之比为 .(用含Q的代数式表示).
考点:反应热和焓变,热化学方程式
专题:化学反应中的能量变化
分析:根据1mol金刚石和石墨分别在氧气中完全燃烧时放出的热量,利用盖斯定律来分析金刚石转化石墨时的能量变化,能量越低的物质越稳定,利用十字交叉法来计算金刚石和石墨的物质的量之比.
解答:
解:由盖斯定律可知,要得到金刚石转化为石墨的热量变化,可将二者在氧气中完全燃烧时放出的热量相减即可,
得C(金刚石)═C(石墨)△H=-395.41kJ/mol-(-393.51kJ/mol)=-1.90kJ/mol,
即金刚石转化为石墨放出热量,说明石墨的能量更低,比金刚石稳定,
金刚石和石墨混合晶体共1mol 在O2中完全燃烧,产生热量为QkJ,
由十字交叉法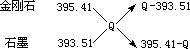 ,
,
可得二者物质的量比为
,
故答案为:C(s,金刚石)═C(s,石墨)△H=-1.9 kJ/mol;石墨;
.
得C(金刚石)═C(石墨)△H=-395.41kJ/mol-(-393.51kJ/mol)=-1.90kJ/mol,
即金刚石转化为石墨放出热量,说明石墨的能量更低,比金刚石稳定,
金刚石和石墨混合晶体共1mol 在O2中完全燃烧,产生热量为QkJ,
由十字交叉法
 ,
,可得二者物质的量比为
| Q-393.5 |
| 395.4-Q |
故答案为:C(s,金刚石)═C(s,石墨)△H=-1.9 kJ/mol;石墨;
| Q-393.5 |
| 395.4-Q |
点评:本题考查学生利用盖斯定律来分析金刚石和石墨的转化,明确反应热、热量、能量与物质的稳定性的关系即可解答,对于混合物的燃烧及成分的确定学生应学会利用十字交叉法来快速解答.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
某溶液中FeCl3的水解反应已达平衡FeCl3+3H2O?Fe(OH)3+3HCl,若要使FeCl3的水解程度增大,应该采用的方法是( )
| A、加入NaHCO3 |
| B、加入AgNO3固体 |
| C、加入FeCl3固体 |
| D、降温 |
下列叙述不正确的是( )
| A、乙烯和植物油都能使酸性高锰酸钾褪色 |
| B、苯、乙酸都可与钠反应生成氢气 |
C、聚乙烯的结构简式为: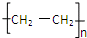 |
| D、灼烧闻气味可以区分棉织物和毛织物 |
下列各组离子能在指定环境中大量共存的是( )
| A、在c(HCO3-)=0.1mol?L-1的溶液中:NH4+、AlO2-、Cl-、NO3- |
| B、在由水电离出的c(H+)=1×10-12mol?L-1的溶液中:Fe2+、ClO-、Na+、SO42- |
| C、在加入铝粉产生H2的溶液中:SO42-、NO3-、Na+、NH4+ |
| D、在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+ |
在元素周期表中位于金属和非金属交界处容易找到的元素是( )
| A、制催化剂的元素 |
| B、制农药的元素 |
| C、半导体元素 |
| D、耐高温的合金元素 |
晶体与非晶体的严格判别可采用( )
| A、有否自范性 |
| B、有否各向同性 |
| C、有否固定熔点 |
| D、有否周期性结构 |
下列有关有机物分子的叙述不正确的是( )
| A、乙烯分子中有一个sp2-sp2σ键和一个p-pπ键 |
| B、乙炔每个碳原子都有两个未杂化的2p轨道,它们之间可形成两个π键 |
| C、乙烷两个C原子均是sp3杂化,分子中一共有6个σ键 |
| D、苯分子中的碳原子采用sp2杂化,且每个碳原子均存在一个未参与杂化的p轨道 |
下列化合物中含有2个手性碳原子的是( )
A、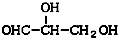 |
B、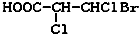 |
| C、CF2Cl2 |
| D、CF2Cl2 |