题目内容
下列实验操作中正确的是( )
| A、配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释 |
| B、倒入漏斗的过滤液的液面应低于滤纸边缘 |
| C、用胶头滴管向试管中加入液体时,为防止滴在试管外面,应将滴管尖嘴处伸入试管口中 |
| D、称量氢氧化钠固体的质量时,将称量物放在纸片上,并置于托盘天平的左盘,砝码放在托盘天平的右盘 |
考点:溶液的配制,计量仪器及使用方法,药品的取用,过滤
专题:实验评价题
分析:A、考虑浓硫酸的稀释和量筒的使用;
B、考虑过滤操作要点;
C、考虑胶头滴管的使用;
D、托盘天平的使用.
B、考虑过滤操作要点;
C、考虑胶头滴管的使用;
D、托盘天平的使用.
解答:
解:A、稀释浓硫酸一定要把浓硫酸注入水中,防止迸溅,量筒量完液体,不能把洗涤液也放在烧杯中,否则造成溶质偏多,故A错误;
B、过滤操作要遵守三低三靠原则,其中之一为过滤液的液面应低于滤纸边缘,故B正确;
C、胶头滴管不能深入试管内,故C错误;
D、氢氧化钠具有腐蚀性,称量时应放在烧杯中称量,故D错误.
故选B.
B、过滤操作要遵守三低三靠原则,其中之一为过滤液的液面应低于滤纸边缘,故B正确;
C、胶头滴管不能深入试管内,故C错误;
D、氢氧化钠具有腐蚀性,称量时应放在烧杯中称量,故D错误.
故选B.
点评:本题考查了实验基本操作,较基础,要熟练掌握实验基本操作知识.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氮原子的氮气在标准状况下的体积约为22.4 L |
| B、标准状况下,11.2 L H2O含有的分子数为0.5NA |
| C、在常温常压下,11.2 L Cl2含有的分子数为0.5NA |
| D、25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L氧气做氧化剂时转移的电子数一定是4NA |
| B、1mol硝基(-NO2)与NA个二氧化氮(NO2)分子所含的电子数相等 |
| C、80 mL 12 mol/L的浓盐酸与足量MnO2反应,生成的Cl2分子数目为0.24NA |
| D、氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
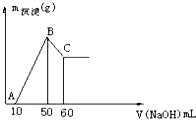 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,下列叙述不正确的是( )
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示,下列叙述不正确的是( )| A、盐酸的物质的量浓度为0.5mol?L-1 |
| B、合金中铝的物质的量为0.01mol |
| C、合金中镁的物质的量为0.005mol |
| D、B点与C点沉淀的物质的量之比为2:1 |
250mL物质的量浓度为2mol?L-1的硫酸溶液,下列说法正确的是( )
| A、取50ml该溶液,含硫酸的物质的量为10mol?L-1 |
| B、含硫酸的物质的量为0.5mol |
| C、含硫酸的物质的量为2mol?L-1 |
| D、含硫酸的物质的量为1mol |
配制一定物质的量浓度的NaOH溶液时,会对实验结果造成影响的是( )
①定容时,加水超过了刻度线,再用胶头滴管将过线的液体吸出
②定容时观察液面俯视
③有少量NaOH溶液残留在烧杯中
④容量瓶中原来有少量蒸馏水.
①定容时,加水超过了刻度线,再用胶头滴管将过线的液体吸出
②定容时观察液面俯视
③有少量NaOH溶液残留在烧杯中
④容量瓶中原来有少量蒸馏水.
| A、①②④ | B、①②③ |
| C、①② | D、②③④ |
将适量的铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则未反应的Fe3+和已反应的Fe3+的物质的量之比是( )
| A、2:3 | B、3:2 |
| C、1:2 | D、1:1 |
配制250mL 0.10mol/L的NaOH溶液时,下列实验操作会使配得的溶液中NaOH物质的量浓度偏大的是( )
| A、转移溶液后未洗涤烧杯和玻璃棒就直接定容 |
| B、溶解后立即转移至容量瓶 |
| C、在容量瓶中定容时俯视刻度线 |
| D、定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水 |

 ),其反应类型是
),其反应类型是