题目内容
16.下列有关能量的叙述不正确的是( )| A. | 活化能的大小对化前后的能量变化不产生影响 | |
| B. | 化学键的断裂和形成是物质在化学变化中发生能量变化的主要原因 | |
| C. | 盐酸和NaOH(aq)反应的中和热△H=-57.3kJ.mol-1,则H2S04(aq)和Ba(0H)2(aq)反应的中 和热△H=2×(-57.3 )kJ•mol-1 | |
| D. | 因 N2(g)+3H2(g)?2NHs(g)△H=-dkJ.mol-1,故在某溶器中投入 l molN2与 3molH2充分反应后,放出热量小于dkJ |
分析 A.活化能的大小对化学反应前后的能量变化不产生影响;
B.根据化学反应中发生能量变化的主要原因是化学键的断裂和形成;
C.中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量;
D.反应为可逆反应.
解答 解:A.活化能的大小对化学反应前后的能量变化不产生影响,故A正确;
B.因化学反应中发生能量变化的主要原因是化学键的断裂和形成,故B正确;
C.中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量,其衡量标准是生成的水为1mol,故无论稀H2SO4和Ca(OH)2反应生成的水是几摩尔,其中和热恒为57.3KJ/mol,故C错误;
D.反应为可逆反应,不能进行到底,放出热量小于dkJ,故D正确.
故选C.
点评 本题考查能量的转换形式,中和热的概念,注意准确把握中和热的概念,题目难度不大.

练习册系列答案
相关题目
7.下列离子方程式不 正确的是( )
| A. | NH4HCO3与足量NaOH混合加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | NH3通入稀H2SO4中:NH3+H+═NH4+ | |
| C. | NaOH和NH4Cl稀溶液混合加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 氨水中加入稀盐酸:NH3•H2O+H+═NH4++H2O |
4.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( )
| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有HClO | |
| D. | 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
11.下列物质具有同分异构体数目最多的是( )
| A. | CH2Cl2 | B. | C4H9Cl | C. | C4H10 | D. | C3H6 |
1.下列有机化合物分子中所有的碳原子都处于问一平面的是( )
| A. | CH3-CH2-CH3 | B. | CH2=CHCH2CH3 | C. | CH3C=CCH2CH3 | D. | 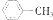 |
8.下列说法正确的是( )
| A. | 次氯酸的结构式:H-Cl-O | |
| B. | 在BF3、PCl5中各元素的最外层都满足8电子稳定结构 | |
| C. | 溴化钙的电子式为:Ca2+[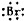 ]${\;}_{2}^{-}$ ]${\;}_{2}^{-}$ | |
| D. | 1molNa2O2中含有3NA个离子(NA表示阿伏加德罗常数) |
5.关于Na2CO3、NaHCO3两种盐的描述错误的是( )
| A. | 可以用加热的方法除去Na2CO3固体中的少量NaHCO3固体 | |
| B. | 可以用澄清石灰水鉴别Na2CO3和NaHCO3两种溶液 | |
| C. | 可以用通CO2气体的方法除去NaHCO3溶液中的Na2CO3 | |
| D. | 饱和Na2CO3溶液中通入CO2气体溶液会出现浑浊 |
6.下列关于置换反应M+X→N+Y其中M、N为单质,X,Y为化合物,反应条件已略去)的说法中正确的是( )
| A. | 若X为氧化物,则Y也一定是氧化物 | |
| B. | 若M为金属单质,则N一定为金属单质 | |
| C. | 若X是不含金属元素的化合物,则N一定是非金属单质 | |
| D. | 若X是含有金属元素的化合物,则Y一定含有金属元素的化合物 |