题目内容
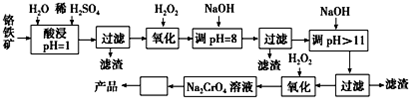
以铬铁矿(主要成分是FeO?Cr2O3,含少量MgCO3、Al2O3、SiO2等)为原料制取铬酸钠(Na2CrO4)晶体的工艺流程如下:
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下.
(1)流程中两次使用了H2O2,分别写出反应的离子方程式: 、 .
(2)加入NaOH调节溶液的pH=8时,被除去的离子是 ;调节溶液的pH>11时,被除去的离子是 .
(3)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么? .
(4)流程图中“□”内的操作是 .

已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO2-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下.
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8 | 9(>9溶解) |
(2)加入NaOH调节溶液的pH=8时,被除去的离子是
(3)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么?
(4)流程图中“□”内的操作是
考点:制备实验方案的设计,难溶电解质的溶解平衡及沉淀转化的本质,物质分离和提纯的方法和基本操作综合应用
专题:实验题,电离平衡与溶液的pH专题
分析:铬铁矿用稀硫酸酸浸,FeO、Cr2O3、MgCO3、Al2O3与硫酸反应加入溶液,而SiO2不反应,过滤除去SiO2.用H2O2将Fe2+氧化为Fe3+,再调节pH=8时,Fe3+、Al3+完全沉淀,过滤得到滤渣为Al(OH)3和Fe(OH)3,再调节pH=11,Mg2+完全沉淀被除去且Cr元素以CrO2-的形式存在,过滤后,向滤液中再加入过氧化氢,将CrO2-氧化为CrO42-,最后采取蒸发浓缩、冷却结晶的方法得到Na2CrO4晶体.
(1)第一次加入H2O2是为了将Fe2+氧化为Fe3+,第二次加入H2O2是为了将CrO2-氧化为CrO42-;
(2)当pH=8时Fe3+、Al3+已完全沉淀,pH>11时,Mg2+完全被除去且Cr元素以CrO2-的形式存在;
(3)“调pH=8”时沉淀成分是Al(OH)3和Fe(OH)3,如果不把前者除去,当继续加入NaOH至pH=11时,Al(OH)3会溶解,引入杂质离子AlO2-;
(4)Na2CrO4溶液得到Na2CrO4晶体,可以采取蒸发浓缩、冷却结晶的方法.
(1)第一次加入H2O2是为了将Fe2+氧化为Fe3+,第二次加入H2O2是为了将CrO2-氧化为CrO42-;
(2)当pH=8时Fe3+、Al3+已完全沉淀,pH>11时,Mg2+完全被除去且Cr元素以CrO2-的形式存在;
(3)“调pH=8”时沉淀成分是Al(OH)3和Fe(OH)3,如果不把前者除去,当继续加入NaOH至pH=11时,Al(OH)3会溶解,引入杂质离子AlO2-;
(4)Na2CrO4溶液得到Na2CrO4晶体,可以采取蒸发浓缩、冷却结晶的方法.
解答:
解:(1)第一次加入H2O2是为了将Fe2+氧化为Fe3+,反应离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O;第二次加入H2O2是为了将CrO2-氧化为CrO42-,反应离子方程式为:2CrO2-+3H2O2+2OH-═2CrO42-+4H2O,
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;2CrO2-+3H2O2+2OH-═2CrO42-+4H2O;
(2)由阳离子转化为氢氧化物完全沉淀的pH数据,可知当pH=8时Fe3+、Al3+已完全沉淀,pH>11时,Mg2+完全被除去且Cr以CrO2-的形式存在,
故答案为:Fe3+、Al3+;Mg2+;
(3)“调pH=8”时沉淀成分是Al(OH)3和Fe(OH)3,如果不把前者除去,当继续加入NaOH至pH=11时,Al(OH)3会溶解,引入杂质离子AlO2-,
故答案为:不能,当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时Al(OH)3会溶解,引入杂质离子AlO2-;
(4)Na2CrO4溶液得到Na2CrO4晶体,可以采取蒸发浓缩、冷却结晶的方法,
故答案为:蒸发浓缩、冷却结晶.
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;2CrO2-+3H2O2+2OH-═2CrO42-+4H2O;
(2)由阳离子转化为氢氧化物完全沉淀的pH数据,可知当pH=8时Fe3+、Al3+已完全沉淀,pH>11时,Mg2+完全被除去且Cr以CrO2-的形式存在,
故答案为:Fe3+、Al3+;Mg2+;
(3)“调pH=8”时沉淀成分是Al(OH)3和Fe(OH)3,如果不把前者除去,当继续加入NaOH至pH=11时,Al(OH)3会溶解,引入杂质离子AlO2-,
故答案为:不能,当pH=8时Al3+已经完全转化为Al(OH)3,若不经过滤除去,当继续加入NaOH时Al(OH)3会溶解,引入杂质离子AlO2-;
(4)Na2CrO4溶液得到Na2CrO4晶体,可以采取蒸发浓缩、冷却结晶的方法,
故答案为:蒸发浓缩、冷却结晶.
点评:本题属于工艺流程制备题目,考查制备原理、实验方案评价、物质分离提纯、获取信息的能力,是对基础知识的综合考查,难度中等.

练习册系列答案
相关题目
在0.1mol?L-1的CH3COOH溶液中存在如下电离平衡CH3COOH?CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
| A、加入少量冰醋酸,溶液的pH减小,CH3COOH的电离度增大 | ||
| B、滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 | ||
| C、加入少量Na2CO3固体,平衡不移动 | ||
D、加水稀释,可使溶液中
|

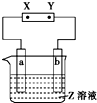
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.依据溴乙烷的性质,请你进行以下探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.依据溴乙烷的性质,请你进行以下探究.

 高炉炼铁中发生的基本反应之一如下:FeO(固)+CO(气)?Fe(固)+CO2(气)(△H>0).
高炉炼铁中发生的基本反应之一如下:FeO(固)+CO(气)?Fe(固)+CO2(气)(△H>0).