题目内容
9.称取NaI和NaCl的混合物10.0克加水溶解,再通入足量的氯气,然后将溶液蒸发至干,强热后得固体6.65克,求混合物中NaCl的质量分数.分析 通入足量氯气发生反应:2NaI+Cl2=2NaCl+I2,然后将溶液蒸发至干,强热后得固体6.65克为NaCl,进而计算NaCl的质量分数.
解答 解:称取NaI和NaCl的混合物10.0克加水溶解,再通入足量的氯气,发生反应:2NaI+Cl2=2NaCl+I2,然后将溶液蒸发至干,强热后得固体6.65克为NaCl,单质碘完全升华,则NaCl的质量分数为$\frac{6.65g}{10g}$×100%=66.5%;
答:混合物中NaCl的质量分数66.5%.
点评 本题考查混合物计算、化学方程式计算,题目难度不大,注意蒸干时碘发生升华,侧重于考查学生的分析能力和计算能力..

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.R是一种激素类药物,结构简式如图所示.下列说法正确的是( )

| A. | R是芳香烃 | B. | R含2种含氧官能团 | ||
| C. | 1mol R最多与1molH2加成 | D. | R能发生加成、取代和氧化反应 |
4.已知在1×105Pa,298K 条件下,2mol 氢气燃烧生成水蒸气放出484kJ 热量,下列热化学方程式正确的是( )
| A. | H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H=242 kJ?mol-1 | B. | 2H2(g)+O2(g)=2H2O(g)△H=-484 kJ?mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(1)△H=-242 kJ?mol-1 | D. | 2H2(g)+O2(g)=2H2O(g)△H=+484 kJ?mol-1 |
1.下列各氢化物中,稳定性按由强到弱的顺序排列的是( )
| A. | AsH3>NH3>PH3 | B. | PH3>AsH3>NH3 | C. | NH3>PH3>AsH3 | D. | NH3>AsH3>PH3 |
18.2016年l月《自然》杂志报道了中科大的研究人员利用直接电解将二氧化碳高效、清洁地转化成液体甲酸燃料的最新成果.下列有关说法正确的是( )
| A. | CO2和HCOOH均属于弱电解质 | B. | CO2和HCOOH均属于有机化合物 | ||
| C. | CO2转变为HCOOH发生还原反应 | D. | 1mol CO2的体积一定等于22.4L |
19.按如图实验,反应后可能出现的现象是( )
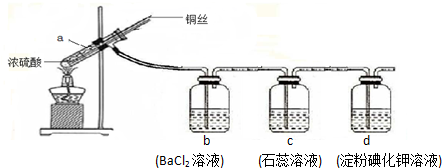

| A. | a装置中有白色固体 | B. | b装置中产生白色沉淀 | ||
| C. | c装置中溶液先变红后褪色 | D. | d装置中溶液变蓝色 |
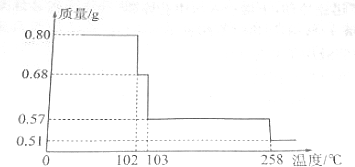
 图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: