题目内容
19.下列分子中所有原子都满足最外层为8电子结构的是( )①BeCl ②NC13 ③PCl5④COC12⑤SF6⑥XeF2⑦CS2⑧CH4⑨CF2C12⑩S2C12.
| A. | ②④⑦⑧⑧⑨⑩ | B. | ②④⑦⑨⑩ | C. | ③④⑦⑩ | D. | ③④⑤⑦⑨⑩ |
分析 共价化合物分子中元素原子最外层电子数+|该元素化合价|(或共价键数目)=8,该元素原子满足8电子结构;
分子中若含有氢元素,则氢原子不能满足最外层8电子稳定结构,但它满足K层为最外层2个电子的稳定结构;
若为同种元素组成的分子,该元素原子的最外层电子数目与其在分子中形成的共价键的数目之和若为8,则其最外层满足8电子结构,反之不满足.
解答 解:①BeCl2分子Be原子最外层电子数为2+2=4,不满足8电子结构,故不选;
②NCl3分子中N原子形成3个N-Cl间,N原子最外层电子数为5+3=8,Cl原子最外层电子数=7+1=8,均满足8电子结构,故选;
③PCl5 分子中P原子最外层电子数为5+5=10,不满足8电子结构,故不选;
④COCl2 分子为C原子与氧原子之间形成C=O双键,C原子与Cl原子之间形成C-Cl,故C原子最外层电子数为4+4=8,Cl原子最外层电子数=7+1=8,O原子最外层电子数6+2=8,均满足8电子结构,故选;
⑤SF6 分子中S原子最外层电子数为6+6=12,不满足8电子结构,故不选;
⑥XeF2 分子中Xe原子本身最外层有8个电子,与F原子形成共价键,分子中最外层电子数大于8,故不选;
⑦CS2 分子中C原子最外层电子数为4+4=8,S原子最外层电子数=6+|-2|=8,均满足8电子结构,故选;
⑧CH4中H原子满足2电子结构,故不选;
⑨CF2Cl2分子中C原子与F、Cl原子之间形成C-F、C-Cl,C原子最外层电子数为4+4=8,Cl原子最外层电子数=7+1=8,F原子最外层电子数7+1=8,均满足8电子结构,故选;
⑩S2Cl2结构式为Cl-S-S-Cl,S原子最外层电子数为6+2=8,Cl原子最外层电子数=7+1=8,均满足8电子结构,故选,
故选:B.
点评 本题考查学生对共价键的理解,掌握8电子结构判断的方法,注意利用化合价(共价键数目)与最外层电子数来分析,难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | KCl=K++Cl- | B. | H2CO3?2 H++CO32- | ||
| C. | H2SO4=2H++SO42- | D. | Ba(OH)2=Ba2++2OH- |
| A. | 在金属钠与足量水反应中,增加水的量能加快反应速率 | |
| B. | 工业生产使用催化剂是为了加快反应速率,提高生产效率 | |
| C. | 2SO2+O2?2SO3反应中,SO2的转化率不能达到100% | |
| D. | 实验室用碳酸钙和盐酸反应制取CO2,用碳酸钙粉末比块状反应要快 |
Ⅰ.请你利用原电池原理,设计实验,比较铜和铁的金属活动性.
实验用品:铁片、铜片、导线、金属夹、小灯泡、硫酸亚铁溶液、硫酸铜溶液、500mL烧杯.
画出实验装置简图,并标出正负极、电子流动方向.
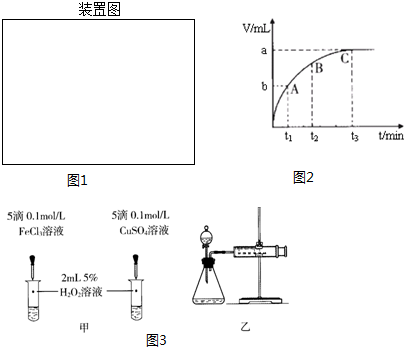
Ⅱ.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入3mL 5% H2O2溶液,各滴入2滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡; 试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入3mL 5% H2O2溶液和3mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
(2)实验①的目的是研究温度对H2O2分解速率的影响.
实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图2所示,则A、B、C三点所表示的瞬时反应速率最慢的是C.
(5)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图3甲、乙所示的实验.请回答相关问题:
①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是排除氯离子的干扰.
②定量分析:用图3乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是收集40mL气体所需的时间.
| 选项 | 待提纯样品(括号内为杂质) | 除杂方法或实验装置 |
| A | 淀粉胶体(KI溶液) | 过滤 |
| B | 乙酸乙酯(饱和碳酸钠溶液) | 蒸馏,收集77℃下馏分 |
| C | CO2(SO2) | 通过盛有饱和碳酸钠溶液的洗气瓶并干燥 |
| D | 氯气(氯化氢) | 通过盛有饱和食盐水的洗气瓶并干燥 |
| A. | A | B. | B | C. | C | D. | D |
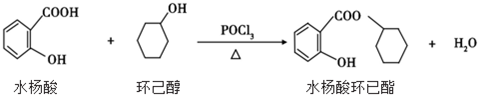
下列说法正确的是( )
| A. | 水杨酸的核磁共振氢谱有 4 个吸收峰 | |
| B. | 水杨酸、环已醇和水杨酸环已酯都能与 FeCl3 溶液发生显色反应 | |
| C. | 1mol 水杨酸跟浓溴水反应时,最多消耗 2molBr2 | |
| D. | 1mol 水杨酸环已酯在 NaOH 溶液中水解时,最多消耗 3molNaOH |
| A. | 制取Fe(OH)3胶体:Fe3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 锅炉除水垢时先用纯碱浸泡:CaSO4+CO32-═CaCO3+SO42- | |
| C. | 泡沫灭火器灭火原理:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| D. | 向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O═CO32-+2C6H5OH |
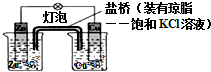
| A. | 正极表面出现气泡 | B. | 电池反应:Zn+Cu2+=Zn2++Cu | ||
| C. | 在外电路中,电流从负极流向正极 | D. | 盐桥中K+移向ZnSO4溶液 |
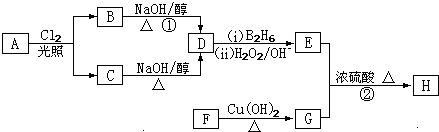
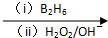 R-CH2CH2OH(B2 H6为乙硼烷)
R-CH2CH2OH(B2 H6为乙硼烷) ;
; ;
;