题目内容
下列各组离子在溶液中按括号内的物质的量之比混合,不能得到无色、碱性、澄清溶液的是( )
| A、Na+、Al3+、Cl-、OH-(5:1:4:4) |
| B、NH4+、Ba2+、OH-、Cl-(1:1:1:2) |
| C、Fe3+、Na+、Cl-、S2-(2:1:5:1) |
| D、K+、H+、I-、HCO3-( 2:1:1:2) |
考点:离子共存问题,离子反应发生的条件
专题:离子反应专题
分析:A.Al3+、OH-以1:4反应生成偏铝酸钠;
B.NH4+、OH-以1:1反应生成一水合氨;
C.Fe3+、S2-发生氧化还原反应;
D.H+、HCO3-结合生成水和气体.
B.NH4+、OH-以1:1反应生成一水合氨;
C.Fe3+、S2-发生氧化还原反应;
D.H+、HCO3-结合生成水和气体.
解答:
解:A.Al3+、OH-以1:4反应生成偏铝酸钠,得到无色、碱性、澄清溶液,故A不选;
B.NH4+、OH-以1:1反应生成一水合氨,得到无色、碱性、澄清溶液,故B不选;
C.Fe3+、S2-发生氧化还原反应生成亚铁离子和S,得到浅绿色溶液,故C选;
D.H+、HCO3-结合生成水和气体,溶液为弱酸性,不是碱性溶液,故D选;
故选CD.
B.NH4+、OH-以1:1反应生成一水合氨,得到无色、碱性、澄清溶液,故B不选;
C.Fe3+、S2-发生氧化还原反应生成亚铁离子和S,得到浅绿色溶液,故C选;
D.H+、HCO3-结合生成水和气体,溶液为弱酸性,不是碱性溶液,故D选;
故选CD.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应是解答本题的关键,题目难度不大,C为学生解答的难点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各组离子可能大量共存的是( )
| A、不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、AlO2- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- |
| D、中性透明溶液:K+、HCO3-、NO3-、Fe3+ |
 有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg
有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg| c(H+) |
| c(OH-) |
| A、A点时加入氢氧化钠溶液体积为20 mL |
| B、室温时0.01 mol?L-1的醋酸溶液pH=6 |
| C、OA段溶液中:c(CH3COO-)>c(CH3COOH) |
| D、若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH)=c(OH-)-c(H+) |
下列叙述正确的是( )
| A、鉴别两种无色溶液Na2CO3与NaHCO3可以用石灰水 |
| B、Mg和Cu的冶炼方法一定要用相同方法:热还原法 |
| C、SO2与CO2对环境污染的原理:均形成酸雨 |
| D、Na2SiO3与Na2O?SiO2是同种物质:都是硅酸盐 |
 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.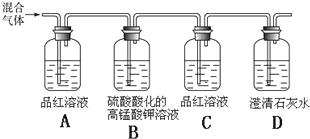
 为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置[已知:酸性H2SO3>H2CO3,Ca(HSO3)2溶于水]:
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置[已知:酸性H2SO3>H2CO3,Ca(HSO3)2溶于水]: