题目内容
0.5molH2SO4中含 个H, mol O, mol电子;8gNaOH与 molBa(OH)2所含OH-相同.
考点:物质的量的相关计算
专题:计算题
分析:根据n=
结合分子的构成计算;计算出8gNaOH所含OH-物质的量,再计算Ba(OH)2的物质的量.
| N |
| NA |
解答:
解:N(H2SO4)=0.5mol×NA/mol=0.5NA,n(O)=4n(H2SO4)=4×0.5mol=2mol;电子数等于质子数,5molH2SO4中,所含电子的物质的量为:0.5mol×(1×2+16+8×4)=25mol;8gNaOH所含OH-物质的量为
=0.2mol,即2×n(Ba(OH)2)=0.2mol,则n(Ba(OH)2)=0.1mol,
故答案为:0.5NA,2,25,0.1.
| 8g |
| 40g/mol |
故答案为:0.5NA,2,25,0.1.
点评:本题考查物质的量的相关计算,难度不大,应熟练应用各种物理量之间的相互转化公式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、C、N、O的第一电离能依次增大 |
| B、NH3、H3O+、NH4+均含有配位键 |
| C、P4、CCl4、CH4均为正四面体结构,键角均为109°28′ |
| D、HClO、HClO3、HClO4的酸性依次增强 |
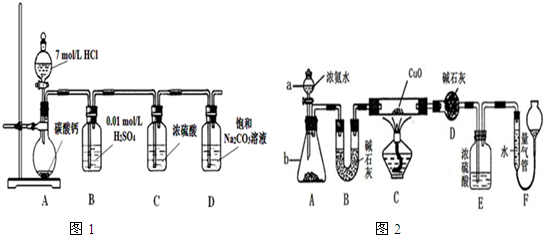
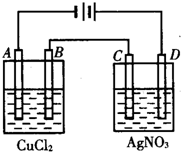 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: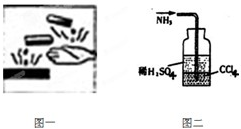 化学是一门以实验为基础的自然科学,进行化学实验时要采取正确的实验操作,注意实验安全:
化学是一门以实验为基础的自然科学,进行化学实验时要采取正确的实验操作,注意实验安全: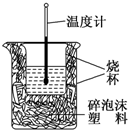 50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: