题目内容
6.下列微粒:Fe、Cl-、H+其中能得到电子的微粒有H+,该元素的化合价+1,表现出氧化性,是氧化剂;具有还原性的微粒是Fe、Cl-,它们在反应中失(填“得”或“失“)电子,发生氧化反应(填”氧化“或”还原“),其化合价升高(填”升高“或”降低“).分析 处于元素最低价的微粒可失去电子具有还原性,处于元素最高价的微粒可得到电子具有氧化性,而处于元素中间价的微粒具有氧化性和还原剂,以此来解答.
解答 解:Fe、Cl-、H+其中能得到电子的微粒有H+,该元素的化合价为-+,表现出氧化性,是氧化剂;具有还原性的微粒是Fe、Cl-,它们在反应中失电子,被氧化,发生氧化反应,其化合价升高,
故答案为:H+;+1;氧化;氧化;Fe、Cl-;失;氧化;升高.
点评 本题考查氧化还原反应,为高频考点,把握微粒的性质与元素化合价的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
16.入夏以来,消防官兵扑灭了黑龙江、内蒙古三起特大森林火灾.开辟防火带(用于防火的通道)是灭火的重要措施之一,在树林中间开辟防火带的主要目的是( )
| A. | 便于消防人员快速通行 | B. | 将可燃物与火源隔离 | ||
| C. | 减少可燃物与空气的接触面积 | D. | 降低可燃物的着火点 |
17.用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 0.5molAl与足量盐酸反应转移电子数为NA | |
| B. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| C. | 0.1 mol CH4所含的电子数为NA | |
| D. | 46gNO2和N2O4的混合物含有的分子数为1NA |
1.下列物质不可以导电的是( )
| A. | 金属Cu | B. | 甲苯 | C. | NaCl溶液 | D. | HCl溶液 |
16. 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )| A. | 莽草酸的分子之间可能发生酯化反应 | |
| B. | 莽草酸的分子式为C7H4O5 | |
| C. | 莽草酸中含有苯环 | |
| D. | 莽草酸不能使溴水褪色 |
17.不能实现下列物质间直接转换的是( )

| A. | 铝 | B. | 碳 | C. | 硫 | D. | 氮 |
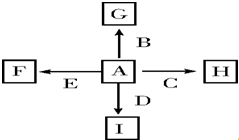 图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.
图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物. 可简写为
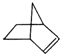
可简写为  .降冰片烯的分子结构可表示为
.降冰片烯的分子结构可表示为