题目内容
3.有一镁铝合金,根据某同学的操作,回答下列问题:①将合金与过量NaOH溶液反应,所得溶液中不存在的离子是B.
A.Na+ B.Mg2+C.OH- D.AlO2-
②将合金溶于过量的盐酸中,充分反应后,溶液中新生成的离子是Mg2+、Al3+.
分析 ①将合金与过量NaOH溶液反应,发生反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,镁不反应;
②将合金溶于过量的盐酸中,发生反应:2Al+6HCl═2AlCl3+3H2↑,Mg+2HCl═MgCl2+H2↑,据此分析.
解答 解:①将合金与过量NaOH溶液反应,发生反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,镁不反应,所以所得溶液中不存在的离子是Mg2+,故选:B;
②将合金溶于过量的盐酸中,发生反应:2Al+6HCl═2AlCl3+3H2↑,Mg+2HCl═MgCl2+H2↑,则溶液中新生成的离子是Mg2+、Al3+,故选:Mg2+、Al3+.
点评 本题考查镁、铝金属的性质,比较简单,注意基础知识的积累.

练习册系列答案
相关题目
13.a g密度为d1 g/cm3质量分数为ω1的硝酸钾溶液,采取某种措施变成bg密度为d2g/cm3质量分数为ω2的硝酸钾饱和溶液,下列表达一定正确的是( )
| A. | a>b | B. | d1>d2 | C. | bω2≥aω1 | D. | a d1ω1=b d2ω2 |
14.下列实验方案正确且能达到相应实验预期目的是( )
| A. | 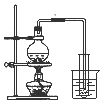 制取少量蒸馏水 | B. |  制取少量NO2 | ||
| C. | 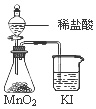 比较MnO2、Cl2、I2的氧化性 | D. |  量取8.50mL的 稀硫酸 |
11.下列各组离子在指定环境中能大量共存的是( )
| A. | 在c(CO32-)=0.1 mol•L-1的溶液中:K+、AlO2-、Cl-、NO3- | |
| B. | 在常温下由水电离出的c(OH-)=1×10-12 mol•L-1的溶液中:Fe2+、ClO-、Na+、SO42- | |
| C. | 在加入苯酚会显紫色的溶液中:NH4+、Cl-、Na+、SCN- | |
| D. | 在能使蓝色石蕊试纸变红的溶液中:S2O32-、CO32-、Na+、K+ |
8. 常温下,向100mL 0.01mol•L-1的HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )
常温下,向100mL 0.01mol•L-1的HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )
 常温下,向100mL 0.01mol•L-1的HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )
常温下,向100mL 0.01mol•L-1的HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )| A. | HA为弱酸 | |
| B. | 常温下,MA溶液的pH>7 | |
| C. | K点对应的溶液中:c(M+)+c(MOH)=c(A-) | |
| D. | 在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OH-)+c(A-) |
15.下列有关CuSO4溶液的叙述正确的是( )
| A. | 通入CO2气体产生蓝色沉淀 | |
| B. | 该溶液中Na+、NH4+、NO3-、Mg2+可以大量共存 | |
| C. | 与H2S反应的离子方程式:Cu2++S2-=CuS↓ | |
| D. | 与过量浓氨水反应的离子方程式:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+ |
12.2011年是国际化学年.中国的宣传口号是“化学--我们的生活.我们的未来”.下列有关叙不正确的是( )
| A. | 在家用燃煤中加人适量的生石灰能有效减少二氧化硫的排放量 | |
| B. | 利用太阳能、潮汐能、风力发电,以获取清洁能源 | |
| C. | 采用纳米二氧化钛光触媒技术.将汽车尾气中的NO和CO转化为无害气体 | |
| D. | 大量排放SO2,NO2或CO2都会导致酸雨的形成 |
13.下列有关实验原理或实验操作正确的是( )
| A. |  此图表示可用蒸馏法分离X、Y | B. |  SO2气体通入溴水中 | ||
| C. |  氨气通入醋酸溶液中 | D. | 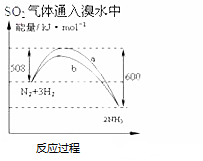 N2(g)+3H2(g)═2NH3(g)△H=-92KJmol |

 .
. ,反应类型是酯化反应(或取代反应).
,反应类型是酯化反应(或取代反应). .
.