题目内容
 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.(1)W在元素周期表中的位置是
(2)工业合成XQ3是放热反应.下列措施中,既能加快反应速率,又能提高原料转化率的是
a.升高温度 b.加入催化剂
c.将XQ3及时分离出去 d.增大反应体系的压强
(3)WQ4Y与Y2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是
(4)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,
Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,则Y是O元素、Z是Na元素;
Q与W组成的化合物是一种温室气体,Q的原子序数小于W,该气体是甲烷,则Q是H元素、W是C元素;
W与Y、X与Y组成的化合物是机动车排出的大气污染物,且X的原子序数大于W而小于Y,所以X是N元素,再结合原子结构、化学平衡、原电池原理解答.
Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,则Y是O元素、Z是Na元素;
Q与W组成的化合物是一种温室气体,Q的原子序数小于W,该气体是甲烷,则Q是H元素、W是C元素;
W与Y、X与Y组成的化合物是机动车排出的大气污染物,且X的原子序数大于W而小于Y,所以X是N元素,再结合原子结构、化学平衡、原电池原理解答.
解答:
解:Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,
Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,则Y是O元素、Z是Na元素;
Q与W组成的化合物是一种温室气体,Q的原子序数小于W,该气体是甲烷,则Q是H元素、W是C元素;
W与Y、X与Y组成的化合物是机动车排出的大气污染物,且X的原子序数大于W而小于Y,所以X是N元素,
(1)W是C元素,C元素在元素周期表中的位置是第二周期第IVA族,Z2Y2是Na2O2,过氧化钠的电子式是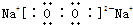 ,故答案为:第二周期第IVA族;
,故答案为:第二周期第IVA族;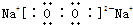 ;
;
(2)工业合成NH3是放热反应,其反应方程式为3H2(g)+N2(g)?2NH3(g)△H<0,
a.升高温度,增大反应速率,但平衡向逆反应方向移动,原料的转化率降低,故错误;
b.加入催化剂能增大反应速率,但平衡不一定,所以原料的转化率不变,故错误;
c.将XQ3及时分离出去,降低反应速率,但转化率增大,故错误;
d.增大反应体系的压强,反应速率增大,且平衡向正反应方向移动,所以能提高原料转化率,故正确;
故选d;
(3)CH3OH与O2的反应可将化学能转化为电能,根据电子流向知,a是负极、b是正极,a电极上通入甲醇,甲醇失电子和氢氧根离子反应生成水和碳酸根离子,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
(4)X和Z组成的一种离子化合物,能与水反应生成两种碱,则该物质是Na3N,Na3N和水反应生成氢氧化钠和一水合氨,所以该反应的化学方程式是Na3N+4H2O=3NaOH+NH3.H2O,故答案为:Na3N+4H2O=3NaOH+NH3.H2O.
Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,则Y是O元素、Z是Na元素;
Q与W组成的化合物是一种温室气体,Q的原子序数小于W,该气体是甲烷,则Q是H元素、W是C元素;
W与Y、X与Y组成的化合物是机动车排出的大气污染物,且X的原子序数大于W而小于Y,所以X是N元素,
(1)W是C元素,C元素在元素周期表中的位置是第二周期第IVA族,Z2Y2是Na2O2,过氧化钠的电子式是
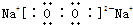 ,故答案为:第二周期第IVA族;
,故答案为:第二周期第IVA族;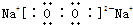 ;
;(2)工业合成NH3是放热反应,其反应方程式为3H2(g)+N2(g)?2NH3(g)△H<0,
a.升高温度,增大反应速率,但平衡向逆反应方向移动,原料的转化率降低,故错误;
b.加入催化剂能增大反应速率,但平衡不一定,所以原料的转化率不变,故错误;
c.将XQ3及时分离出去,降低反应速率,但转化率增大,故错误;
d.增大反应体系的压强,反应速率增大,且平衡向正反应方向移动,所以能提高原料转化率,故正确;
故选d;
(3)CH3OH与O2的反应可将化学能转化为电能,根据电子流向知,a是负极、b是正极,a电极上通入甲醇,甲醇失电子和氢氧根离子反应生成水和碳酸根离子,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
(4)X和Z组成的一种离子化合物,能与水反应生成两种碱,则该物质是Na3N,Na3N和水反应生成氢氧化钠和一水合氨,所以该反应的化学方程式是Na3N+4H2O=3NaOH+NH3.H2O,故答案为:Na3N+4H2O=3NaOH+NH3.H2O.
点评:本题考查了位置结构性质的相互关系及应用,涉及原电池原理、化学平衡移动等知识点,正确推断元素是解本题关键,再结合原电池原理、化学平衡移动及反应速率的影响因素分析解答,题目难度中等.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数,以下说法错误的是( )
| A、25℃,1.01×105Pa时,4g氦气所含的原子个数为NA |
| B、0.1 mol的OH-中所含电子个数为NA |
| C、120 g由NaHSO4和KHSO3组成的混合物中含有的硫原子数为NA |
| D、8.4 g的NaHCO3中含有的阳离子个数为0.2NA |
下列电子式书写正确的是( )
A、 |
B、 |
C、 |
D、 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1 molCl2与足量Fe反应转移电子数一定为2NA |
| B、常态下,11.2 LCO2和O2混合气体中含NA个氧原子 |
| C、1L 0.1mol/LFeCl3溶液可制备0.1NA个Fe(OH)3胶粒 |
| D、0.1mol/L的醋酸溶液中含有0.1NA个H+ |
NA为阿伏加德罗常数,下列叙述正确的是( )
| A、80g硝酸铵中含有氮原子数为NA |
| B、在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| C、2mol金属铝与足量的盐酸反应,共失去了4NA个电子 |
| D、16 g氧气和16 g臭氧所含的原子数均为NA |
 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用胶头滴管滴入5ml盐酸于试管中,试回答下列问题:
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用胶头滴管滴入5ml盐酸于试管中,试回答下列问题: