题目内容
20.某化学小组为了验证放热反应和吸热反应,他们设计如图所示装置.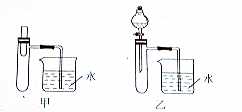
回答下列问题:
(1)根据烧杯中的导管有气泡冒出,验证2Na202+2H20=4Na0H+02↑是放热反应,他们选择乙装置,你认为是否可行?不可行(填“可行”或“不可行”),简述理由:Na202与H20反应放出02,导管有气泡冒出.
(2)选择甲装置进行如下实验:
在小试管中加人少量的过氧化钠和含酚酞的水,观察到的现象是小试管中溶液先变红色,过一会儿,溶液褪色;如果烧杯中不再产生气泡,装置冷却后还观察到的现象是导管中产生水柱.
分析 (1)反应放热,空气膨胀,空气逸出,导管有气泡冒出,Na202与H20反应放出02,导管有气泡冒出;
(2)Na202与H20反应生成Na0H,碱能使酚酞变红;Na202与H20反应生成Na0H和02,反应放热,空气膨胀,空气逸出,冷却后压强减小.
解答 解:(1)反应放热,空气膨胀,空气逸出,导管有气泡冒出,Na202与H20反应放出02,导管有气泡冒出,所以烧杯中的导管有气泡冒出,不能确定反应放热;
故答案为:不可行;Na202与H20反应放出02,导管有气泡冒出;
(2)Na202与H20反应生成Na0H,碱能使酚酞变红;Na202与H20反应生成Na0H和02,反应放热,空气膨胀,空气逸出,冷却后压强减小,导管中产生水柱;
故答案为:红;导管中产生水柱.
点评 本题考查了探究放热反应的方法,题目难度中等,试题主要侧重实验方案的设计与评价.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
10.向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )


| A. | a点对应的溶液中:Na+、OH-、SO42-、NO3- | |
| B. | b点对应的溶液中:H+、Al3+、NO3-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:Cl-、NO3-、Fe2+、Na+ |
11.某同学在实验室进行铁盐与亚铁盐相互转化的实验:
实验Ⅰ:将Fe3+转化为Fe2+(图1)
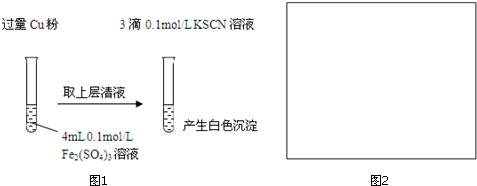
(1)Fe3+与Cu粉发生反应的离子方程式为2Fe3++Cu═2Fe2++Cu2+.
(2)探究白色沉淀产生的原因,请填写实验方案:
查阅资料:
ⅰ.SCN-的化学性质与I-相似,ⅱ.2Cu2++4I-=2CuI↓+I2
Cu2+与SCN-反应的离子方程式为2Cu2++4SCN-=2CuSCN↓+(SCN)2.
实验Ⅱ:将Fe2+转化为Fe3+
探究上述现象出现的原因:
查阅资料:Fe2++NO?Fe(NO)2+(棕色)
(3)用离子方程式解释NO 产生的原因3Fe2++4H++NO3-═3Fe3++NO↑+2H2O.
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应Ⅰ:Fe2+与HNO3反应; 反应Ⅱ:Fe2+与NO反应
①依据实验现象,甲认为反应Ⅰ的速率比反应Ⅱ慢(填“快”或“慢”).
②乙认为反应Ⅰ是一个不可逆反应,并通过实验证明其猜测正确,乙设计的实验方案是取反应后的黄色溶液于试管中,向其中加入几滴K3[Fe(CN)6]溶液,溶液无明显变化,说明反应I是不可逆反应.
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因Fe2+被硝酸氧化为Fe3+,导致溶液中Fe2+浓度降低,导致平衡Fe2++NO?Fe(NO)2+逆向移动,最终Fe(NO)2+完全转化为Fe3+,溶液由棕色变为黄色.
(5)丙认为若生成的NO与Fe2+不接触,溶液就不会出现棕色,请设计实验方案,并画出实验装置图2,实现
Fe2+$\stackrel{稀HNO_{3}}{→}$Fe3+的转化,同时避免出现此异常现象.
实验Ⅰ:将Fe3+转化为Fe2+(图1)

(1)Fe3+与Cu粉发生反应的离子方程式为2Fe3++Cu═2Fe2++Cu2+.
(2)探究白色沉淀产生的原因,请填写实验方案:
查阅资料:
ⅰ.SCN-的化学性质与I-相似,ⅱ.2Cu2++4I-=2CuI↓+I2
| 实验方案 | 现象 | 结论 |
| 步骤1:取4mL0.1mol/L CuSO4溶液,向其中滴加3滴0.1mol/L KSCN溶液 | 产生白色沉淀 | CuSO4与KSCN反应产生了白色沉淀 |
| :步骤2:取取4mL 0.1mol/L FeSO4溶液,向其中滴加3滴0.1mol/L KSCN溶液 | 无明显现象 |
实验Ⅱ:将Fe2+转化为Fe3+
| 实验方案 | 现象 |
| 向3mL 0.1mol/L FeSO4溶液中加入1mL 8mol/L稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
查阅资料:Fe2++NO?Fe(NO)2+(棕色)
(3)用离子方程式解释NO 产生的原因3Fe2++4H++NO3-═3Fe3++NO↑+2H2O.
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应Ⅰ:Fe2+与HNO3反应; 反应Ⅱ:Fe2+与NO反应
①依据实验现象,甲认为反应Ⅰ的速率比反应Ⅱ慢(填“快”或“慢”).
②乙认为反应Ⅰ是一个不可逆反应,并通过实验证明其猜测正确,乙设计的实验方案是取反应后的黄色溶液于试管中,向其中加入几滴K3[Fe(CN)6]溶液,溶液无明显变化,说明反应I是不可逆反应.
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因Fe2+被硝酸氧化为Fe3+,导致溶液中Fe2+浓度降低,导致平衡Fe2++NO?Fe(NO)2+逆向移动,最终Fe(NO)2+完全转化为Fe3+,溶液由棕色变为黄色.
(5)丙认为若生成的NO与Fe2+不接触,溶液就不会出现棕色,请设计实验方案,并画出实验装置图2,实现
Fe2+$\stackrel{稀HNO_{3}}{→}$Fe3+的转化,同时避免出现此异常现象.
15.将3mol的NO2气体依次通入下列三个分别装有足量①NaHCO3饱和溶液 ②浓H2SO4 ③Na2O2的装置后,用排水法把残留气体收集起来,则收集到的气体是(同温、同压下测定)( )
| A. | 1 mol NO | B. | 1 mol NO2和0.05 mol O2 | ||
| C. | 2 mol O2 | D. | 0.25 mol O2 |
5.标准状态下,在三个干燥的烧瓶中分别充入:①纯净的氨气,②纯净的NO2气体,③NO2和O2按4:1混合而成的气体.然后各做喷泉实验.实验后,三个烧瓶中溶液的物质的量浓度之比为( )
| A. | 5:5:4 | B. | 2:1:2 | C. | 1:1:1 | D. | 无法确定 |
12.下面的叙述正确的是( )
| A. | 使湿润淀粉-KI试纸变蓝色的气体必为氯气 | |
| B. | 氟气与熔融状态下氯化钠反应可产生氯气 | |
| C. | 易见光分解的AgNO3晶体,应存放于棕色细口试剂瓶中 | |
| D. | 溴水应存放在胶头滴瓶(棕色)中 |
9.茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示,下列说法正确的是( )

| A. | X难溶于乙醇 | |
| B. | 酒中的少量丁酸能抑制X的水解 | |
| C. | 分子式为C4H8O2且官能团与X相同的物质共有5种 | |
| D. | X完全燃烧后生成CO2和H20的物质的量比为1:2. |
19. 常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知Ksp(CaSO4)=9×10-6.下列说法不正确的是( )
常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知Ksp(CaSO4)=9×10-6.下列说法不正确的是( )
 常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知Ksp(CaSO4)=9×10-6.下列说法不正确的是( )
常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知Ksp(CaSO4)=9×10-6.下列说法不正确的是( )| A. | a点对应的Ksp等于c点对应的Ksp | B. | 加入Na2SO4溶液可以使a点变为b点 | ||
| C. | a点变为b点将有沉淀生成 | D. | d点未达到沉淀溶解平衡状态 |
