题目内容
Na2FeO4是一种高效多功能水处理剂,应用前景广阔,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法不正确的是( )
| A、Na2O2在反应中只作氧化剂 |
| B、O2是氧化产物 |
| C、Na2FeO4既是氧化产物又是还原产物 |
| D、2 mol FeSO4发生反应时,共有8 mol电子转移 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑中,Fe元素的化合价由+2价升高为+6价,过氧化钠中O元素的化合价既升高又降低,以此来解答.
解答:
解:A.过氧化钠中O元素的化合价既升高又降低,则既是氧化剂又是还原剂,故A错误;
B.过氧化钠中O元素的化合价升高,生成氧气,则氧气为氧化产物,故B正确;
C.Fe元素的化合价升高,过氧化钠中O元素的化合价降低,对应的Na2FeO4既是氧化产物又是还原产物,故C正确;
D.由反应可知,2molFeSO4发生反应时,由化合价变化可知转移电子为2mol×(6-2)+2mol×[(-1)-(-2)]=10mol,故D错误;
故选AD.
B.过氧化钠中O元素的化合价升高,生成氧气,则氧气为氧化产物,故B正确;
C.Fe元素的化合价升高,过氧化钠中O元素的化合价降低,对应的Na2FeO4既是氧化产物又是还原产物,故C正确;
D.由反应可知,2molFeSO4发生反应时,由化合价变化可知转移电子为2mol×(6-2)+2mol×[(-1)-(-2)]=10mol,故D错误;
故选AD.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列氧化还原反应中,水作为还原剂的是( )
| A、2F2+2H2O=4HF+O2 | ||||
| B、3NO2+H2O=2HNO3+NO | ||||
| C、2Na+2H2O=2NaOH+H2↑ | ||||
D、C+H2O
|
在无色透明的强酸性溶液中,能大量共存的离子组是( )
| A、K+、SO42-、CO32-、Na+ |
| B、Ca2+、NO3-、Al3+、Cl- |
| C、Fe3+、Cu2+、K+、OH- |
| D、MnO4-、K+、SO42-、Na+ |
向某无色溶液中分别进行下列操作,所得现象和结论正确的是( )
| A、加入氨水,产生白色沉淀,证明原溶液中存在Al3+ |
| B、加入AgNO3溶液,产生白色沉淀,证明原溶液中存在Cl- |
| C、加入盐酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中存在SO42- |
| D、加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH4+ |
对于可逆反应A(g)+3B(g)?2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是( )
| A、v(A)=0.5 mol?L-1?min-1 |
| B、v(B)=1.2 mol?L-1?s-1 |
| C、v(D)=0.4 mol?L-1?min-1 |
| D、v(C)=0.1 mol?L-1?s-1 |
下列说法是否正确?( )
①将 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2
②乙酰水扬酸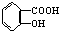 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备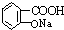
③从煤焦油中分离出苯、甲苯、二甲苯等有机物的过程为化学变化
④实验时手指不小心沾上苯酚,立即用70°以上的热水清洗.
①将
 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2②乙酰水扬酸
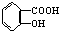 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备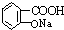
③从煤焦油中分离出苯、甲苯、二甲苯等有机物的过程为化学变化
④实验时手指不小心沾上苯酚,立即用70°以上的热水清洗.
| A、都不正确 | B、只有①③正确 |
| C、只有②④正确 | D、都正确 |
食品卫生与身体健康密切相关,下列做法中对人体健康不会造成危害的是( )
| A、用甲醛浸泡海鲜 |
| B、用硫磺薰制白木耳 |
| C、用小苏打做发酵粉 |
| D、用工业酒精兑制白酒 |
在一定条件下,反应N2+3H2═2NH3在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为( )
| A、v(H2)=0.03mol?L-1?min-1 |
| B、v(N2)=0.02mol?L-1?min-1 |
| C、v(NH3)=0.17mol?L-1?min-1 |
| D、v(NH3)=0.01mol?L-1?min-1 |
