题目内容
3.反应2A(g)+B(g)?2C(g)△H<0.下列反应条件有利于生成C的是( )| A. | 低温、低压 | B. | 低温、高压 | C. | 高温、高压 | D. | 高温、低压 |
分析 该反应是气体体积减小、放热的可逆反应,要使该反应向正反应方向移动,可采取加压、降低温度、减小C的浓度、增加反应物的浓度的方法.
解答 解:反应2A(g)+B(g)?2C(g)△H<0.该反应是气体体积减小、放热的可逆反应,要使该反应向正反应方向移动,可采取加压、降低温度、减小C的浓度、增加反应物的浓度的方法.
故选B.
点评 本题考查了化学平衡的影响因素,难度不大,注意压强对反应前后气体体积不变的反应无影响.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
18.在由Fe、FeO和Fe2O3组成的混合物中加入100ml 2mol/L的盐酸,恰好使混合物完全溶解,并放出448mL气体(标准状况),此时溶液中滴入KSCN溶液无明显变化,则下列判断正确的是( )
| A. | 混合物里三种物质反应时消耗盐酸的物质的量之比为1:1:3 | |
| B. | 反应后所得溶液中的Fe3+与的物质的量之比为1:3 | |
| C. | 混合物里FeO的物质的量无法确定,但Fe和Fe2O3的物质的量多 | |
| D. | 混合物里Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
19.对于反应8NH3+3Cl2═N2+6NH4Cl,下列说法正确的是( )
| A. | N2是还原产物,且还原剂与氧化剂物质的量之比是2:3 | |
| B. | N2是氧化产物,且还原剂与氧化剂物质的量之比是2:3 | |
| C. | 每转移6mol电子就生成22.4LN2 | |
| D. | NH4Cl是氧化产物,且还原剂与氧化剂物质的量之比是2:3 |
16.下列微粒的基态电子排布式一定错误的是( )
| A. | A原子:1s22s22p63s23p63d10 | B. | B2-:1s22s22p6 | ||
| C. | C2+:1s22s22p6 | D. | D原子:1s22s22p6 |
8.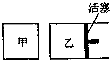 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为a%,乙容器中SO2的转化率为b%,则a与b的关系为( )
 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为a%,乙容器中SO2的转化率为b%,则a与b的关系为( )
| A. | a>b | B. | a=b | C. | a<b | D. | 无法确定 |
15. 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
发生如下反应:CO(g)+H2O (g)═CO2(g) 十 H2 (g);△H<0
(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率v(CO2)=0.03mol•L-1•min-1
(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如表:
计算t1℃该反应的平衡常数K=0.5.
(3)t2℃时,化学反应CO (g)+H2O (g)?CO2(g)+H2 (g)的平衡浓度符合c(CO2)•c(H2)═2c(CO)•c(H2O),则t2℃<850℃,判断依据是:t2℃的平衡常数为2,大于850℃的平衡常数1,平衡右移
(4)在t1℃达平衡时,又充入CO,再次平衡时,混合气体中H2O的体积分数将减小(填“增大”、“减小”或“无法确定”) H2O的转化率将增大(填“增大”、“减小”或“无法确定”)
(5))判断该反应达到化学平衡状态的依据是AB(填序号):
A.V(正)(CO)=V (逆)(CO2)
B.CO消耗速率等于H2的消耗速率
C. 容器内压强保持不变
D.混合气体的密度保持不变
E.容器中气体的平均相对分子质量不随时间而变化
F.混合气体的质量保持不变.
 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO(g)+H2O (g)═CO2(g) 十 H2 (g);△H<0
(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率v(CO2)=0.03mol•L-1•min-1
(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如表:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
(3)t2℃时,化学反应CO (g)+H2O (g)?CO2(g)+H2 (g)的平衡浓度符合c(CO2)•c(H2)═2c(CO)•c(H2O),则t2℃<850℃,判断依据是:t2℃的平衡常数为2,大于850℃的平衡常数1,平衡右移
(4)在t1℃达平衡时,又充入CO,再次平衡时,混合气体中H2O的体积分数将减小(填“增大”、“减小”或“无法确定”) H2O的转化率将增大(填“增大”、“减小”或“无法确定”)
(5))判断该反应达到化学平衡状态的依据是AB(填序号):
A.V(正)(CO)=V (逆)(CO2)
B.CO消耗速率等于H2的消耗速率
C. 容器内压强保持不变
D.混合气体的密度保持不变
E.容器中气体的平均相对分子质量不随时间而变化
F.混合气体的质量保持不变.
12.下列由实验现象得出的结论正确的是:( )
| 选项 | 操作及现象 | 结论 |
| A | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 溶液中含有NH4+ |
| B | 将浓硝酸滴入碳酸钠溶液中,然后将生成的气体直接通入硅酸钠溶液中,溶液变浑浊. | 酸性:硝酸>碳酸>硅酸 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,溶液变成蓝色 | 氧化性:I2>Cl2 |
| D | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| A. | A | B. | B | C. | C | D. | D |
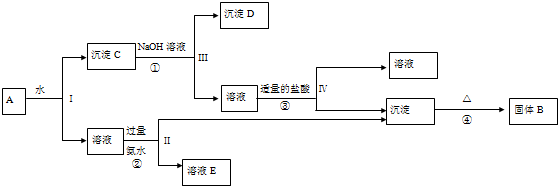
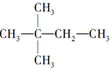 ,则A的结构简式为(CH3)3CCH=CH2.
,则A的结构简式为(CH3)3CCH=CH2.