题目内容
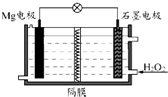 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图所示.该电池工作时,下列说法错误的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图所示.该电池工作时,下列说法错误的是( )| A、Mg电极是该电池的负极 |
| B、溶液中Cl-向石墨电极移动 |
| C、该装置中电子从Mg电极流向石墨电极 |
| D、H2O2在石墨电极上发生还原反应 |
考点:化学电源新型电池
专题:电化学专题
分析:镁、过氧化氢和海水形成原电池,镁做负极发生氧化反应,过氧化氢在正极上发生还原反应,过氧化氢做氧化剂被还原为水,原电池中阴离子移向负极,电子从负极流向正极,据此回答判断.
解答:
解:A、组成的原电池的负极被氧化,镁为负极,故A正确;
B、溶液中Cl-移动方向同外电路电子移动方向一致,应向负极方向移动,即向着镁极移动,故B错误;
C、该装置中电子从负极Mg电极流向正极石墨电极,故C正确;
D、双氧水作为氧化剂,在石墨上被还原变为水,发生还原反应,故D正确.
故选B.
B、溶液中Cl-移动方向同外电路电子移动方向一致,应向负极方向移动,即向着镁极移动,故B错误;
C、该装置中电子从负极Mg电极流向正极石墨电极,故C正确;
D、双氧水作为氧化剂,在石墨上被还原变为水,发生还原反应,故D正确.
故选B.
点评:本题考查了原电池原理的分析判断,电极名称、电极反应、电子流向等知识,熟记教材知识是解题关键,题目难度中等.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
反应4A(s)+3B(g)═2C(g)+D(g),经2min,B的浓度减少0.6mol?L-1,对此反应速率的表示,正确的是( )
| A、A的浓度减少了0.8mol?L-1 |
| B、分别用B、C、D表示的反应速率其比值为1:1:1 |
| C、在2min末的反应速率,用B表示是0.3mol?L-1?min-1 |
| D、在这2min内用B和C表示的反应速率都是逐渐减小的 |
为了配制c(NH4+):c(C1-)=1:1的NH4C1溶液,可在NH4C1溶液中加入( )
①适量的HCl ②适量的NaCl ③适量的氨水
④适量的NaOH ⑤加水 ⑥适量的(NH4)2CO3.
①适量的HCl ②适量的NaCl ③适量的氨水
④适量的NaOH ⑤加水 ⑥适量的(NH4)2CO3.
| A、③ | B、①②③④ |
| C、⑤⑥ | D、②③⑥ |
下列离子方程式书写正确的是( )
| A、碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O |
| B、向氢氧化钠溶液中通入过量二氧化碳:OH-+CO2=HCO3- |
| C、澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| D、铁钉放入硫酸铜溶液中:Fe+3Cu2+=2Fe3++3Cu |
已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则下列说法中正确的是( )
| A、浓硫酸和NaOH溶液反应,生成1mol水时放热57.3kJ |
| B、含1mol H2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ |
| C、1L 0.1mol/L CH3COOH与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ |
| D、1L 0.1 mol/L HNO3与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ |
下列说法正确的是( )
| A、胶体与其它分散系的本质区别是有丁达尔效应,而其它分散系没有 |
| B、胶体粒子的直径小于1nm |
| C、丁达尔效应可用于鉴别胶体和溶液 |
| D、胶粒能通过滤纸,也能通过半透膜 |
在由水电离出的c(H+)=10-13mol?L-1的溶液中一定能够大量存在的离子组是( )
| A、Ba2+、Na+、Cl-、NO3- |
| B、Al3+、Ca2+、SO42-、Br- |
| C、NH4+、K+、HSO3-、CO32- |
| D、Na+、K+、Cl-、I- |
下列能表示阿伏加德罗常数数值的是( )
| A、1molH2含有的电子数 |
| B、通常状况下,22.4LCO2所含的分子数 |
| C、0.012kg12C所含的原子数 |
| D、1LO.5mol?L-1的CaCl2溶液所含的Cl-数 |
常温下,下列各组离子在给定条件下能大量共存的是( )
| A、在pH=1的溶液中:NH4+、K+、Ba2+、Cl- |
| B、在滴加石蕊试液显红色的溶液中:K+、NH4+、CO32-、SO42- |
| C、有NO3-存在的溶液中:H+、Ba2+、Cl-、SO32- |
| D、在c(H+)=1.0×10-3mol?L-1的溶液中:Na+、K+、SO42-、[Al(OH)4]- |