题目内容
实验室用NaOH固体配制480ml 1.0mol/L的NaOH溶液,填空并请回答问题:
(1)配制480mL 1.0mol/L的NaOH溶液
(2)容量瓶上标有以下五项中的 ;
①浓度 ②温度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A、将容量瓶盖紧,颠倒摇匀
B、用天平准确称取所需的NaOH的质量,加入少量水(约200ml),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、用50ml水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)下列配制的溶液浓度偏低的是 ;
A、称量NaOH时,砝码错放在左盘(注:1g以下用游码,以本题计算结果判断)
B、向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C、定容时俯视刻度线
D、加蒸馏水时不慎超过了刻度线
E、配制前,容量瓶中有少量蒸馏水.
(1)配制480mL 1.0mol/L的NaOH溶液
| 应称取NaOH的质量 | 应选用容量瓶的规格 | 除容量瓶外还需要的其它玻璃仪器 |
①浓度 ②温度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A、将容量瓶盖紧,颠倒摇匀
B、用天平准确称取所需的NaOH的质量,加入少量水(约200ml),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、用50ml水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)下列配制的溶液浓度偏低的是
A、称量NaOH时,砝码错放在左盘(注:1g以下用游码,以本题计算结果判断)
B、向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C、定容时俯视刻度线
D、加蒸馏水时不慎超过了刻度线
E、配制前,容量瓶中有少量蒸馏水.
考点:配制一定溶质质量分数、物质的量浓度溶液的方法
专题:
分析:(1)根据m=nM=cvM计算溶质的质量;根据溶液的体积确定容量瓶的规格;根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)根据容量瓶上标有:规格、温度和刻度线;
(3)根据实验操作的步骤;
(4)根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断.
(2)根据容量瓶上标有:规格、温度和刻度线;
(3)根据实验操作的步骤;
(4)根据c=
| n |
| V |
解答:
解:(1)溶质的质量m=nM=cvM=1mol/L×0.5L×40g/mol=20g,配制500mL溶液,则选用容量瓶的规格为500mL,配制时步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以还需要的仪器为烧杯、玻璃棒、胶头滴管,
故答案为:20;500;烧杯、玻璃棒、胶头滴管;
(2)因容量瓶上标有:规格、温度和刻度线,故答案为:②③⑤;
(3)配制时步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,故答案为:BCDFEA;
(4)A、称量NaOH时,砝码错放在左盘,溶质的质量减少,浓度偏小,故A正确;
B、向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面,溶质的质量减少,浓度偏小,故B正确;
C、定容时俯视刻度线,溶液体积偏小,浓度偏大,故C错误;
D、加蒸馏水时不慎超过了刻度线,溶液体积偏大,浓度偏小,故D正确;
E、配制前,容量瓶中有少量蒸馏水,无影响,浓度不变,故E错误;
故答案为:ABD.
故答案为:20;500;烧杯、玻璃棒、胶头滴管;
(2)因容量瓶上标有:规格、温度和刻度线,故答案为:②③⑤;
(3)配制时步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,故答案为:BCDFEA;
(4)A、称量NaOH时,砝码错放在左盘,溶质的质量减少,浓度偏小,故A正确;
B、向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面,溶质的质量减少,浓度偏小,故B正确;
C、定容时俯视刻度线,溶液体积偏小,浓度偏大,故C错误;
D、加蒸馏水时不慎超过了刻度线,溶液体积偏大,浓度偏小,故D正确;
E、配制前,容量瓶中有少量蒸馏水,无影响,浓度不变,故E错误;
故答案为:ABD.
点评:本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意实验的基本操作方法和注意事项.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
电解水时为了增强其导电性不应加入的电解质是( )
| A、 | B、 | C、 |
利用金属活性的不同,可以采取不同的冶炼方法冶炼金属.下列反应所描述的冶炼方法不可能实现的是( )
A、2Al2O3(熔融)
| ||||
B、Fe2O3+3CO
| ||||
| C、Fe+CuSO4═FeSO4+Cu | ||||
D、AL+3MgO
|
X、Y、Z三种元素原子的核电荷数在10~18之间,它们的最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4.则下列判断正确的是( )
| A、非金属性:X<Y<Z |
| B、含氧酸的酸性:H3ZO4>H2YO4>HXO4 |
| C、气态氢化物稳定性:按X、Y、Z顺序增加 |
| D、元素电负性:按X、Y、Z变小 |
下列反应中,生成物的总能量大于反应物总能量的是( )
| A、氢气在氧气中燃烧 |
| B、锌和稀硫酸反应制取氢气 |
| C、盐酸和氢氧化钠的中和反应 |
| D、焦炭在高温下与水蒸气反应 |
下列叙述中正确的是( )
| A、元素周期表中有18个纵行,所以有18个族 |
| B、除第一周期外,其他周期均有18个元素 |
| C、副族元素中没有非金属元素 |
| D、碱金属元素是指ⅠA族的所有元素 |
氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:
H2(g)+O2(g)=H2O(l)△H=-285.8kJ/mol
CO(g)+O2(g)=CO2(g)△H=-283.0kJ/mol
C8H18(l)+O2(g)=8CO2(g)+9H2O(l)△H=-5518kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
H2(g)+O2(g)=H2O(l)△H=-285.8kJ/mol
CO(g)+O2(g)=CO2(g)△H=-283.0kJ/mol
C8H18(l)+O2(g)=8CO2(g)+9H2O(l)△H=-5518kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
| A、H2 (g) |
| B、CO(g) |
| C、C8H18 (l) |
| D、CH4(g) |
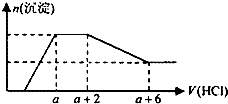 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子.当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图象如图所示.下列说法正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子.当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图象如图所示.下列说法正确的是( )| A、原溶液中一定含有的阴离子是:OH-、SiO32-、AlO2-、CO32- |
| B、反应最后形成的溶液中的溶质为NaCl |
| C、原溶液中一定含有Na2SO4 |
| D、原溶液中含有CO32-与AlO2- 的物质的量之比为1:2 |