题目内容
7.设NA表示阿伏加德罗常数,下列说法不正确的是( )| A. | 1mol醋酸的质量与NA个醋酸分子的质量相等 | |
| B. | NA个氧气分子和NA个氢气分子的质量比等于16:1 | |
| C. | 30g乙烷(C2H6)所含的原子数目为NA | |
| D. | 在标准状况下,0.5NA个氯气分子所占体积约是11.2L |
分析 A、NA个即为1mol,m=n×M;
B、NA个即为1mol,利用m=n×M来计算质量比;
C.物质的量n=$\frac{m}{M}$,1个乙烷分子中含有8个原子;
D、标准状况下,Vm=22.4L/mol,V=n×Vm.
解答 解:A、NA个即为1mol,由m=n×M可知,1mol醋酸的质量与NA个醋酸分子的质量相等,故A正确;
B、NA个氧分子和NA个氢分子的质量比等于1mol×32g/mol:1mol×2g/mol=16:1,故B正确;
C.30g乙烷(C2H6)物质的量=$\frac{30g}{30g/mol}$=1mol,所含的原子数目为8NA,故C错误;
D、在标准状况下,0.5NA个氯气分子,其物质的量为0.5mol,则体积为0.5mol×22.4L/mol=11.2L,故D正确;
故选C.
点评 本题考查阿伏加德罗常数,题目难度不大,注意物质的组成、结构、性质和存在条件是否标准状态以及物质的聚集状态等问题,解答此类题目时,常从以上几个角度考虑.

练习册系列答案
相关题目
17.下列化学用语的书写正确的是( )
| A. | 羟基的电子式: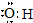 | |
| B. | 过氧化氢的电子式: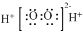 | |
| C. | As的原子的特征电子排布式:[Ar]4s14p3 | |
| D. | 基态Mg原子的核外电子排布图: |
15.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe2+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生沉淀;过滤、洗涤、灼烧,得到1.6g红棕色固体;向上述滤液中加入足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在4种离子 | |
| B. | Cl-一定存在,且c(Cl )≥0.4 mol/L | |
| C. | SO42-、NH4+,一定存在,Cl-可能不存在 | |
| D. | CO32-、Al3+一定不存在,K+可能存在 |
2.在化合物C3H9N的分子中,N原子以三个单键与其它原子相连接,则化合物C3H9N具有的同分异构体的数目为( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
16.下列有关硅及其化合物的说法中正确的是( )
| A. | 硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中 | |
| B. | 反应①Na2SiO3+H2O+CO2═Na2CO3+H2SiO3↓,反应②Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$NaSiO3+CO2↑,两反应是相互矛盾的,不可能都发生 | |
| C. | 普通玻璃、石英玻璃、水泥等均属于硅酸盐材料 | |
| D. | 祖母绿的主要成分为Be3Al2Si6O18,用氧化物形式表示为3BeO•Al2O3•6SiO2 |
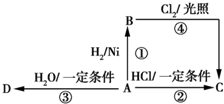 某烃A是有机化学工业的基础原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.
某烃A是有机化学工业的基础原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.