题目内容
在一定条件下,N2和O2于密闭容器中发生如下反应:2N2(g)+O2(g)?2N2O(g).下列说法能说明该反应达到化学平衡状态的有( )
| A、反应不再进行 |
| B、反应体系中的c(N2)不再发生变化 |
| C、c(N2O)=c(N2) |
| D、N2O的分解速率与生成速率相等 |
考点:活化能及其对化学反应速率的影响
专题:化学平衡专题
分析:化学反应到达平衡时,正逆反应速率相等,各物质的物质的量浓度不再发生变化来进行判断.
解答:
解:A、反应达到平衡状态时,正逆反应速率相等但反应不停止且反应速率不为0,故A错误;
B、化学反应到达平衡时,各物质的物质的量浓度不再发生变化,故B正确;
C、化学反应到达平衡时,各物质的物质的量浓度不再发生变化,但是不一定是相等的,故C错误;
D、N2O的分解速率与生成速率相等,说明正逆反应速率相等,达到了平衡,故D正确.
故选BD.
B、化学反应到达平衡时,各物质的物质的量浓度不再发生变化,故B正确;
C、化学反应到达平衡时,各物质的物质的量浓度不再发生变化,但是不一定是相等的,故C错误;
D、N2O的分解速率与生成速率相等,说明正逆反应速率相等,达到了平衡,故D正确.
故选BD.
点评:本题考查平衡状态的判断,对于反应前后气体的计量数之和不相等的可逆反应来说,可从浓度、温度、颜色、压强、百分含量等角度判断是否达到平衡状态.

练习册系列答案
相关题目
短周期元素X、Y、Z、Q、R,原子序数依次增大.X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素.
由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
B(在水溶液中进行);已知C是溶于水显酸性的气体;D是淡黄色固体.下列叙述错误的是( )
由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
| C |
| D |
A、D的电子式为: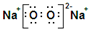 |
| B、X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质的分子式为:C2H2 |
| C、五种元素原子半径由大到小的顺序是:Q>R>Y>Z>X |
| D、A转化为B的离子方程式一定是:2AlO2-+3H2O+CO2→2Al(OH)3↓+CO32- |
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )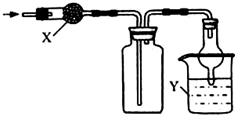

| 选项 | X | 收集气体 | Y |
| A | 碱石灰 | 氯化氢 | 水 |
| B | 碱石灰 | 氨气 | 水 |
| C | 氯化钙 | 二氧化硫 | 氢氧化钠 |
| D | 氯化钙 | 一氧化氮 | 氢氧化钠 |
| A、A | B、B | C、C | D、D |
食用醋中含有乙酸.下列关于乙酸的说法正确的是( )
| A、结构简式为:C2H4O2 |
| B、分子式为:CH3COOH |
| C、可与金属Na反应生成H2 |
| D、分子中原子之间只存在单键 |
 如图是可逆反应X+Y?Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是 ( )
如图是可逆反应X+Y?Z 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是 ( )| A、t1时,只有正方向反应 |
| B、t2-t3,各物质的浓度相等 |
| C、t2-t3,反应不再发生 |
| D、t2时,达到该条件下的反应限度 |
已知A、B、C均为短周期的元素,A、B同周期、A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构,下列说法正确的是( )
| A、C元素的最高正价为+7价 |
| B、离子半径:A2->C->B2+ |
| C、对应气态氢化物的稳定性:A>C |
| D、还原性:A2->C- |
常温下,0.1mo1?L-1的某酸HR溶液的pH=3,下列叙述正确的是( )
| A、若将其加水稀释至原来体积的10倍,则pH=4 |
| B、与NaOH溶液反应的离子方程式:H++OH-=H2O |
| C、常温下,HR的电离平衡常数约为10-5 |
| D、与等体积pH=11的NaOH溶液混合后所得溶液显碱性 |
由乙醇制取乙二酸乙二酯,最简单的流程途径顺序正确的是( )
①取代反应;
②加成反应;
③氧化反应;
④还原反应;
⑤消去反应;
⑥酯化反应;
⑦中和反应.
①取代反应;
②加成反应;
③氧化反应;
④还原反应;
⑤消去反应;
⑥酯化反应;
⑦中和反应.
| A、①②③⑤⑦ |
| B、⑤②①③⑥ |
| C、⑤②①③⑦ |
| D、①②⑤③⑥ |