题目内容
5.在2L的密闭容器中,充入1mol N2和3molH2,在一定条件下反应,2分钟后达到平衡状态,相同温度下,测得平衡时混和气体的压强比反应前混和气体的压强减小了$\frac{1}{10}$,填写下列空白:(1)平衡时混合气体中N2、H2和NH3的物质的量之比:2:6:1
(2)2分钟内,NH3的平均反应速率为:0.1mol/(L﹒min)
(3)反应前和平衡时混合气体的平均摩尔质量之比为:9:10.
分析 根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量.
令参加反应的氮气的物质的量为nmol,则:
N2 +3H2 ?2NH3 ,
开始(mol):1 3 0
变化(mol):n 3n 2n
平衡(mol):1-n 3-3n 2n
压强之比等于物质的量之比,所以(1-n+3-3n+2n)mol=(1+3)mol×(1-$\frac{1}{10}$),解得n=0.2,以此解答该题.
解答 解:令参加反应的氮气的物质的量为nmol,则:
N2 +3H2 ?2NH3 ,
开始(mol):1 3 0
变化(mol):n 3n 2n
平衡(mol):1-n 3-3n 2n
压强之比等于物质的量之比,所以(1-n+3-3n+2n)mol=(1+3)mol×(1-$\frac{1}{10}$),解得n=0.2,
(1)平衡时n(N2)=(1-n)mol=(1-0.2)mol=0.8mol
平衡时n(H2)=(3-3n)mol=(3-3×0.2)mol=2.4mol
平衡时n(NH3)=2n=0.2mol×2=0.4mol,
则平衡时混合气体中N2、H2和NH3的物质的量之比0.8:2.4:0.4=2:6:1,
故答案为:2:6:1;
(2)2分钟内,NH3的平均反应速率为$\frac{\frac{0.4mol}{2L}}{2min}$=0.1mol/(L﹒min),
故答案为:0.1mol/(L﹒min);
(3)气体的质量不变,则反应前后的气体的摩尔质量之比与物质的量成反比,为(1+3-0.4):(1+3)=9:10,故答案为:9:10.
点评 本题考查化学平衡的有关计算,为高考常见题型,侧重考查学生的分析能力和计算能力,题目涉及主要是反应速率,转化率等概念的理解应用,难度不大,注意基础知识的掌握与三段式解题法的运用.

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 工业合成氨时采用铁触媒作反应的催化剂 | |
| C. | 工业生产硫酸的过程中使用过量的空气以提高SO2的转化率 | |
| D. | 将收集NO2气体的烧瓶密闭后放在装有热水的烧杯中,发生颜色变化 |
| A. | 容量瓶中有少量蒸馏水 | |
| B. | 溶液从烧杯转移到容量瓶后没有洗涤烧杯 | |
| C. | 未冷却即将溶液转移到容量瓶 | |
| D. | 定容时俯视容量瓶刻度线 |
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:1.6×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加(填“增加”、“减小”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填>、<或=).
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定上述反应速率,得到c(NH2COO-)随时间变化趋势如图所示.
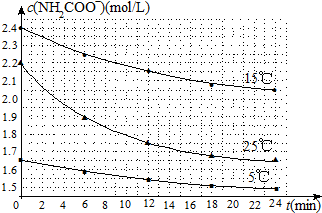
⑤计算25℃时,0~6min上述反应中氨基甲酸铵的平均速率0.05mol/(L•min).
⑥根据图中信息,如何说明上述反应速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
| A. | 催化剂 | B. | 浓度 | C. | 压强 | D. | 温度 |