题目内容
废旧材料的回收利用有仅可以节约资源,产生新的经济效益,而且可以减少对环境的污染.下面是从一种含有A1、Li、Co的新型电子材料的废料中回收某种钴的氧化物的工艺流程(已知:废料中A1以金属锃箔的形式存在,钴以Co2O3?CoO的形式吸附于铝箔表面,Li混杂于其中.):
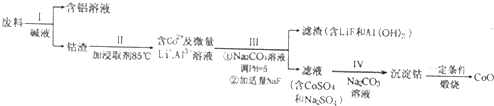
(1)过程I中采用NaOH溶液溶解废料中的铝,反应的化学反应方程式为 .
(2)过程Ⅱ酸化,再加入Na2S2O3溶液浸出钴(已知反应后的溶液中只有一种酸根离子),写出浸出钴的离子方程式 .
(3)过程Ⅲ加入Na2CO3溶液在沉淀铝时起到重要作用,写出其反应的离子方程式 .
(4)已知常温下,Na2CO3溶液水解平衡常数为:Kb1=1×10-7;Kb2=1×10-11,Co(OH)2的溶度积为:Ksp 2×10-15,CoCO3的溶度积为:Ksp=1×10-13,则向0.1
mol/L的Na2CO3溶液中逐滴加入0.1mol/L CoSO4溶液,开始生成的沉淀为(写化学式) .工艺流程中过程Ⅳ生成沉淀的离子方程式为 .

(1)过程I中采用NaOH溶液溶解废料中的铝,反应的化学反应方程式为
(2)过程Ⅱ酸化,再加入Na2S2O3溶液浸出钴(已知反应后的溶液中只有一种酸根离子),写出浸出钴的离子方程式
(3)过程Ⅲ加入Na2CO3溶液在沉淀铝时起到重要作用,写出其反应的离子方程式
(4)已知常温下,Na2CO3溶液水解平衡常数为:Kb1=1×10-7;Kb2=1×10-11,Co(OH)2的溶度积为:Ksp 2×10-15,CoCO3的溶度积为:Ksp=1×10-13,则向0.1
mol/L的Na2CO3溶液中逐滴加入0.1mol/L CoSO4溶液,开始生成的沉淀为(写化学式)
考点:物质分离和提纯的方法和基本操作综合应用
专题:
分析:废料用碱液溶解,过滤得到偏铝酸钠溶液和钴渣;用硫酸溶解钴渣,发生反应:4Co3O4+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,得到含有钴离子的溶液,然后调节溶液pH并用碳酸钠溶液除去杂质铝离子,得到较纯净的含有钴离子的溶液,再加入碳酸钠、调节溶液的pH将钴离子转化成碳酸钴沉淀,最后灼烧碳酸钴得到氧化钴,
(1)铝和氢氧化钠反应生成偏铝酸钠和氢气;
(2)Co3O4和Na2S2O3在酸性条件下发生氧化还原反应生成CoSO4、Na2SO4和H2O,反应方程式为:4Co2O3?CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,
(3)Na2CO3溶液水解呈碱性,可促进铝离子的水解生成氢氧化铝沉淀和二氧化碳气体;
(4)向0.1摩尔/升的碳酸钠溶液中逐底加入0.1摩尔/升CoSO4溶液,碳酸钠溶液呈碱性,但碱性较小,溶液中碳酸根离子浓度远远大于氢氧根离子浓度,开始生成的沉淀为CoCO3.
(1)铝和氢氧化钠反应生成偏铝酸钠和氢气;
(2)Co3O4和Na2S2O3在酸性条件下发生氧化还原反应生成CoSO4、Na2SO4和H2O,反应方程式为:4Co2O3?CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,
(3)Na2CO3溶液水解呈碱性,可促进铝离子的水解生成氢氧化铝沉淀和二氧化碳气体;
(4)向0.1摩尔/升的碳酸钠溶液中逐底加入0.1摩尔/升CoSO4溶液,碳酸钠溶液呈碱性,但碱性较小,溶液中碳酸根离子浓度远远大于氢氧根离子浓度,开始生成的沉淀为CoCO3.
解答:
解:废料用碱液溶解,过滤得到偏铝酸钠溶液和钴渣;用硫酸溶解钴渣,发生反应:4Co3O4+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,得到含有钴离子的溶液,然后调节溶液pH并用碳酸钠溶液除去杂质铝离子,得到较纯净的含有钴离子的溶液,再加入碳酸钠、调节溶液的pH将钴离子转化成碳酸钴沉淀,最后灼烧碳酸钴得到氧化钴,
(1)铝和氢氧化钠反应生成偏铝酸钠和氢气,反应的方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)由流程可知,Co2O3?CoO经酸化后加入Na2S2O3溶液可生成Co2+和SO42-,反应的离子方程式为4Co2O3?CoO+S2O32-+22H+=12Co2++2SO42-+11H2O,
故答案为:4Co2O3?CoO+S2O32-+22H+=12Co2++2SO42-+11H2O;
(3)Na2CO3溶液水解呈碱性,可促进铝离子的水解生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑,
故答案为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;
(4)向0.1摩尔/升的碳酸钠溶液中逐底加入0.1摩尔/升CoSO4溶液,碳酸钠溶液呈碱性,但碱性较小,溶液中CO32->>远远大于c(OH-),溶液中钴离子浓度相等,所以Q(CoCO3)≈0.1×0.1=0.01>Ksp(CoCO3)、Q[Co(OH)2]<Ksp[Co(OH)2],开始生成的沉淀为CoCO3,
过程Ⅳ中碳酸根离子和钴离子反应生成碳酸钴沉淀,离子方程式为Co2++CO32-═CoCO3↓,
故答案为:CoCO3;Co2++CO32-═CoCO3↓.
(1)铝和氢氧化钠反应生成偏铝酸钠和氢气,反应的方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)由流程可知,Co2O3?CoO经酸化后加入Na2S2O3溶液可生成Co2+和SO42-,反应的离子方程式为4Co2O3?CoO+S2O32-+22H+=12Co2++2SO42-+11H2O,
故答案为:4Co2O3?CoO+S2O32-+22H+=12Co2++2SO42-+11H2O;
(3)Na2CO3溶液水解呈碱性,可促进铝离子的水解生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑,
故答案为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;
(4)向0.1摩尔/升的碳酸钠溶液中逐底加入0.1摩尔/升CoSO4溶液,碳酸钠溶液呈碱性,但碱性较小,溶液中CO32->>远远大于c(OH-),溶液中钴离子浓度相等,所以Q(CoCO3)≈0.1×0.1=0.01>Ksp(CoCO3)、Q[Co(OH)2]<Ksp[Co(OH)2],开始生成的沉淀为CoCO3,
过程Ⅳ中碳酸根离子和钴离子反应生成碳酸钴沉淀,离子方程式为Co2++CO32-═CoCO3↓,
故答案为:CoCO3;Co2++CO32-═CoCO3↓.
点评:本题考查物质的分离和提纯,涉及难溶物的溶解平衡、氧化还原反应等知识点,综合性较强,侧重考查分析、计算、推断能力,明确实验原理是解本题关键,知道流程图中发生的反应,会正确书写方程式,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
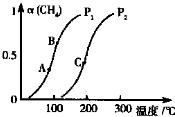 天然气在工农业生产中具有重要意义.
天然气在工农业生产中具有重要意义.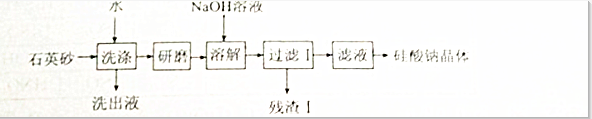

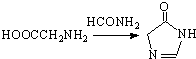
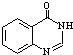 .合成过程中无机试剂任选;合成路线流程图示例为:CH3CH2OH
.合成过程中无机试剂任选;合成路线流程图示例为:CH3CH2OH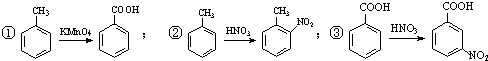
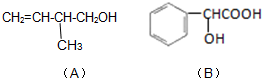 已知有机化合物A和B的结构简式分别为
已知有机化合物A和B的结构简式分别为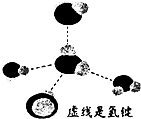 元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,
元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子, 用中和滴定法测定某烧碱样品的纯度.有以下步骤:
用中和滴定法测定某烧碱样品的纯度.有以下步骤: