题目内容
12.1.01×105Pa,150℃时,将1L C2H4、2L C2H6与20L氧气混合并点燃,完全反应后氧气有剩余.当反应后的混合气体恢复到原条件时,气体体积为( )| A. | 15L | B. | 20L | C. | 23L | D. | 24L |
分析 150℃,水为气体,燃烧的化学方程式为C2H4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O(g)反应前后气体的体积不变,2C2H6+7O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+6H2O(g),2L C2H6燃烧消耗7L氧气,
以此来解答.
解答 解:150℃,水为气体,燃烧的化学方程式为C2H4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O(g)反应前后气体的体积不变,2C2H6+7O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+6H2O(g),2L C2H6燃烧消耗7L氧气,生成10的气体,所以反应后体积增加1体积,则当反应后的混合气体恢复到原条件时,气体体积为1+2+20+1=24,故选D.
点评 本题考查化学反应方程式的计算,为高频考点,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
3.下列有关物质性质的说法正确的是( )
| A. | 热稳定性:HCl<HBr<HI | B. | 原子半径:K<Na<Li | ||
| C. | 熔点:Cl2>Br2>I2 | D. | 氧化性:Cl2>Br2>I2 |
20.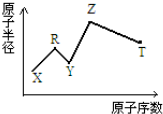 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 简单的气态氢化物的沸点和稳定性排序均为:Y>T | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
7.在下列元素中,不属于主族元素的是( )
| A. | 铁 | B. | 钙 | C. | 磷 | D. | 碘 |
17.2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g)是制备硫酸的重要反应.下列叙述中,正确的是( )
| A. | 催化剂V2O5不改变该反应的逆反应速率 | |
| B. | 增大反应体系的压强,反应速率不一定增大 | |
| C. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1mol/L、c2mol/L,则时间间隔t1min~t2min内,SO3(g)生成的平均速率为v=$\frac{{c}_{2}-{c}_{1}}{{t}_{2}-{t}_{1}}$mol/L•min |