题目内容
13.向试管b分别滴加入a中物质,下列对b中现象的解释错误的是( )| 实验 | a中物质 | b中现象 | 结论或解释 | |
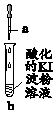 | A. | Fe(OH)3悬浊液 | Fe(OH)3悬浊液溶解,溶液变蓝 | 发生反应:2Fe(OH)3+6H++2I-=2Fe2++6H2O+I2 |
| B. | NaClO3溶液 | 先变蓝后褪色 | 褪色的反应:2ClO3-+10I-+12H+═Cl2+5I2+6H2O | |
| C. | \ | 空气中放置一段时间,溶液变蓝 | 发生反应:4I-+4H++O2=2I2+2H2O | |
| D. | 含碘元素的无色溶液 | 溶液呈蓝色 | 可能发生的反应:5I-+IO3-+6H+=3I2+3H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铁离子的氧化性大于碘单质,铁离子能够将碘离子氧化成碘单质;
B.氯酸钠氧化性大于碘单质,碘单质被氧化成碘酸,溶液褪色;
C.酸性条件下碘离子被空气中氧气氧化成碘单质,溶液变蓝;
D.IO3-与碘离子在酸性条件下发生反应生成碘单质,使溶液变蓝.
解答 解:A.氢氧化铁与酸反应生成的铁离子具有氧化性,能够将碘离子氧化成碘单质,试题淀粉溶液变蓝,发生反应为:2Fe(OH)3+6H++2I-=2Fe2++6H2O+I2,故A正确;
B.溶液褪色的原因是生成的碘单质被NaClO3溶液氧化成碘酸,正确的反应为:5ClO3-+3H2O+3I2═6IO3-+5Cl-+6H+,故B错误;
C.空气中放置一段时间,酸性条件下碘离子与空气中氧气发生反应:4I-+4H++O2=2I2+2H2O,所以溶液变蓝,故C正确;
D.酸性条件下IO3-与I-发生的反应:5I-+IO3-+6H+=3I2+3H2O,所以溶液会变蓝,故D正确;
故选B.
点评 本题考查了化学实验方案的评价,题目难度中等,明确溶液褪色或变蓝的实质为解答关键,注意熟练掌握常见元素及其化合物性质,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.黑火药爆炸时的反应为:S+2KNO3+3C$\frac{\underline{\;点燃\;}}{\;}$K2S+N2↑+3CO2↑.该反应的还原剂是( )
| A. | C | B. | S | C. | KNO3 | D. | S和KNO3 |
1.在一定条件下,苯与氯气在氯化铁催化下连续反应,生成以氯苯、氯化氢为主要产物,邻二氯苯、对二氯苯为次要产物的粗氯代苯混合物.有关物质的沸点、熔点如下:
下列说法不正确的是( )
| 氯苯 | 邻二氯苯 | 对二氯苯 | |
| 沸点/℃ | 132.2 | 180.5 | 174 |
| 熔点/℃ | -45.6 | -15 | 53 |
| A. | 该反应属于取代反应 | |
| B. | 反应放出的氯化氢可以用水吸收 | |
| C. | 用蒸馏的方法可将邻二氯苯从有机混合物中首先分离出来 | |
| D. | 从上述两种二氯苯混合物中,用冷却结晶的方法可将对二氯苯分离出来 |
8.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol甲醇分子中含有的共价键数为4 NA | |
| B. | 7.8g Na2O2固体与水完全反应时,转移的电子数为0.1NA | |
| C. | 标准状况下,11.2 L水中含有的氧原子数为0.5 NA | |
| D. | 1 L 0.5 mol/L CH3COONa溶液中含有的CH3COO-数为0.5 NA |
18.下列物质中,既能发生水解反应又能发生氢化反应的是( )
| A. | 甘油 | B. | 植物油 | C. | 乙酸乙酯 | D. | 高级脂肪酸 |
5.既可以用来鉴别乙烯和甲烷,又可以用来除去甲烷中混有的乙烯的最好方法是( )
| A. | 点燃 | B. | 与酸性高锰酸钾溶液反应 | ||
| C. | 通入足量的溴水 | D. | 在催化剂存在的条件下与氢气反应 |
2.下列解释过程或事实的方程式不正确的是( )
| A. | 氨气遇浓盐酸产生白烟:NH3+HCl═NH4Cl | |
| B. | 打磨过的铝片与NaOH溶液反应产生气体:2Al+2OH-═2AlO2-+H2↑ | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | Fe(OH)2由白色变灰绿,最后变为红褐色:4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
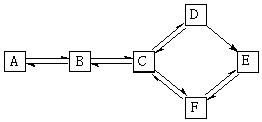 有A、B、C、D、E、F六种有机化合物,存在下图所示转化关系.已知A属于烃,且相对分子质量不超过30;在加热条件下,B可与氢氧化钠溶液反应,向反应后所得液中加入过量的硝酸,再加入硝酸银溶液,生成淡黄色沉淀.
有A、B、C、D、E、F六种有机化合物,存在下图所示转化关系.已知A属于烃,且相对分子质量不超过30;在加热条件下,B可与氢氧化钠溶液反应,向反应后所得液中加入过量的硝酸,再加入硝酸银溶液,生成淡黄色沉淀.