题目内容
在3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O反应中.
(1)每生成2mol的NO,有 mol的稀硝酸被还原.
(2)当有19.2g Cu参加反应时,消耗硝酸的总量为 mol,被还原的硝酸为 mol.
(3)当生成标况下的NO 22.4L时,被还原的硝酸是 mol.
(1)每生成2mol的NO,有
(2)当有19.2g Cu参加反应时,消耗硝酸的总量为
(3)当生成标况下的NO 22.4L时,被还原的硝酸是
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:在3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素化合价由0价升高到+2价,N元素化合价由+5价降低到+2价,反应中硝酸起到氧化剂和酸的作用,结合反应的化学方程式计算该题.
解答:
解:(1)反应N元素化合价由+5价降低到+2价,硝酸被还原生成NO,则每生成2mol的NO,有2mol的稀硝酸被还原,故答案为:2;
(2)n(Cu)=
=0.3mol,由方程式可知,有0.8mol硝酸参加反应,其中被还原的硝酸为0.2mol,
故答案为;0.8;0.2;
(3)n(NO)=
=1mol,
则被还原的硝酸为1mol,
故答案为:1.
(2)n(Cu)=
| 19.2g |
| 64g/mol |
故答案为;0.8;0.2;
(3)n(NO)=
| 22.4L |
| 22.4L/mol |
则被还原的硝酸为1mol,
故答案为:1.
点评:本题考查氧化还原反应的计算,侧重于学生的分析能力和计算能力的考查,为高频考点,注意根据元素的化合价的变化结构反应的方程式计算该题,难度不大.

练习册系列答案
相关题目
角鲨烯是一种高度不饱和烃类化合物,最初是从鲨鱼的肝脏中发现的,分子中含有多个双键,分子式为C30H50,具有生物氧化还原作用,从而增强机体的耐力与改善心脏功能,可用于癌症的防治,是一种无毒性的具有防病治病作用的海洋生物活性物质.下列叙述中正确的是( )
①能使KMnO4酸性溶液褪色
②能与氢气发生加成反应
③角鲨烯只含碳、氢两种元素
④角鲨烯易被氧化.
①能使KMnO4酸性溶液褪色
②能与氢气发生加成反应
③角鲨烯只含碳、氢两种元素
④角鲨烯易被氧化.
| A、①②③ | B、①③④ |
| C、②③④ | D、①②③④ |
下列说法正确的是( )
| A、蛋白质、淀粉、纤维素和油脂都是高分子有机物 |
| B、苯和乙酸乙酯都能发生取代反应 |
| C、煤干馏可得苯及甲苯等,是由于煤中含有苯及甲苯等物质 |
| D、淀粉、纤维素和蛋白质水解都生成葡萄糖 |
下列说法正确的是( )
| A、强电解质一定是离子化合物 |
| B、强酸、强碱及大部分盐类是强电解质 |
| C、强电解质的饱和溶液一定是浓溶液 |
| D、强电解质在水中一定能全部溶解 |
 (Ⅰ)已知:H+(aq)+OH-(aq)═H2O(l)△H1=-57.3kJ/mol
(Ⅰ)已知:H+(aq)+OH-(aq)═H2O(l)△H1=-57.3kJ/mol 工业上常用天然气作为制备甲醇CH3OH的原料.已知:
工业上常用天然气作为制备甲醇CH3OH的原料.已知:
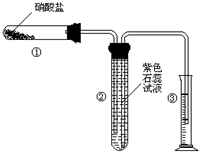 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)
某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)