题目内容
18.下列说法正确的是( )①一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率但不影响生成H2的总量,可向盐酸中加入适量的Na2SO4溶液
②一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是:加入少量CuSO4固体
③对于某反应X+3Y=3E+2F,在甲、乙、丙、丁四种不同条件下分别测得反应速率为甲:V(X)=0.3mol/(L.min);乙:V(Y)=1.2mol/(L.min);丙:V(E)=0.8mol/(L.min);丁:V(F)=0.9mol/(L.min),则反应最快的是乙
④在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,Z的浓度有可能为0.3mol/L.
| A. | ①②③ | B. | .①②④ | C. | ②③④ | D. | 全部正确 |
分析 ①降低反应物浓度、降低温度都能减缓反应速率;
②原电池能加快反应速率;
③同一反应中不同物质的化学反应速率与其计量数之比越大该反应速率越快;
④采用极限法计算Z浓度.
解答 解:①降低反应物浓度、降低温度都能减缓反应速率,该反应中Fe过量、稀盐酸一定量,加入适量硫酸钠溶液后混合溶液体积增大,氢离子浓度降低导致反应速率降低,且Fe和硫酸钠不反应生成氢气,所以减缓反应速率且不影响生成H2的总量,故正确;
②原电池能加快反应速率,该反应中Zn过量、稀盐酸一定量,Zn和硫酸铜发生置换反应生成Cu,Zn、Cu和电解质溶液构成原电池加快反应速率,且氢离子总物质的量不变,所以生成氢气总量不变,故正确;
③同一反应中不同物质的化学反应速率与其计量数之比越大该反应速率越快,甲:$\frac{V(X)}{1}$=0.3mol/(L.min)、乙:$\frac{V(Y)}{3}$=$\frac{1.2}{3}$ mol/(L.min)=0.4 mol/(L.min)、丙:$\frac{V(E)}{3}$=$\frac{0.8}{3}$ mol/(L.min)=0.27 mol/(L.min)、丁:$\frac{V(F)}{2}$=$\frac{0.9}{2}$ mol/(L.min)=0.45 mol/(L.min),所以反应速率大小顺序是丁>乙>甲>丙,所以反应速率最快的是丁,故错误;
④如果Z完全转化为X2、Y2,则Z的浓度为0,如果X2完全转化为Z,则生成Z物质的量浓度是0.2mol/L,加上原来的Z,所以共有0.4mol/L,实际上这几种物质都有,所以Z的浓度为0-0.4mol/L之间,所以当反应达到平衡时,Z的浓度有可能为0.3mol/L,故正确;
故选B.
点评 本题考查化学平衡计算及化学反应速率影响因素,为高频考点,明确化学反应原理及化学平衡计算方法是解本题关键,侧重考查学生理解、分析、计算能力,注意①②中限制性条件“改变反应速率但不影响生成氢气总量”,注意:原电池能加快反应速率.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案(1)写出工业合成氨的化学方程式N2(g)+3H2(g)?2NH3(g).
(2)若0.5mol N2完全反应生成NH3可放出(填“吸收”或“放出”)热量46kJ.
(3)如果将0.5mol N2和1.5mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是该反应是可逆反应,反应物不能完全转化为生成物,所以放出的热量要小于46kJ.
(4)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过5min后,数据如下,则用N2表示的化学反应速率为0.4mol/L/min.
| 物质 | N2 | H2 | NH3 |
| 反应前 | 16mol | xmol | 0 |
| 5min | ymol | 28mol | 8mol |
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
f.反应达到最大限度.
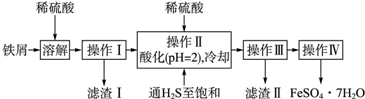
| 25℃时 | pH[] |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)操作Ⅱ中,通入硫化氢至饱和的目的是除去溶液中的Sn2+;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀,并防止Fe2+被氧化.
(2)滤渣Ⅱ的主要成分是SnS.
(3)操作Ⅳ得到的绿矾晶体用少量冰水此空删去洗涤,其目的是:此空删去
①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.010 00mol•L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①滴定时盛放KMnO4溶液的仪器为酸式滴定管(填仪器名称).
②判断此滴定实验达到终点的方法是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色.
③计算上述样品中FeSO4•7H2O的质量分数为97.5%.
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500 s内N2O5分解速率为296×10-3mol•L-1•s-1 | |
| B. | 该温度下的反应平衡时N2O5的转化率为29.6% | |
| C. | 1000s后,其它条件不变,将容器的体积压缩到原来的$\frac{1}{2}$,则c(N2O5)<5.00mol/L | |
| D. | 反应达平衡后,其他条件不变,升高温度平衡常数将增大 |
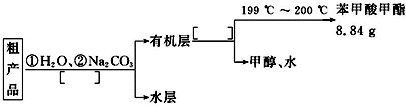
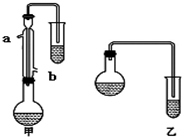 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
(2)实验中浓硫酸的作用是催化剂、吸水剂.
(3)反应物CH3OH应过量,理由是反应物CH3OH过量,使平衡向右移动,有利于提高苯甲酸的转化率.
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称.