题目内容
下列说法中,正确的是( )
| A、向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| B、取相同浓度的NaCl溶液和NaClO溶液,NaCl溶液中离子的总浓度大于NaClO溶液中离子的总浓度 |
| C、某盐的溶液呈酸性,该盐一定发生了水解反应 |
| D、pH相同的盐酸和氯化铵溶液中由水电离出的c(H+)相同 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:A.NaHCO3溶液与NaAlO2溶液混合产生白色沉淀氢氧化铝;
B.结合电荷守恒判断;
C.盐溶液呈酸性,可能有两种情况,一是水解呈酸性,为强酸弱碱盐,二是酸式盐,电离程度大于水解程度,或只有电离;
D.盐酸抑制了水的电离,氯化铵中铵离子促进了水的电离;
B.结合电荷守恒判断;
C.盐溶液呈酸性,可能有两种情况,一是水解呈酸性,为强酸弱碱盐,二是酸式盐,电离程度大于水解程度,或只有电离;
D.盐酸抑制了水的电离,氯化铵中铵离子促进了水的电离;
解答:
解:A.向NaAlO2溶液中滴加饱和NaHCO3溶液,偏铝酸根离子促进碳酸氢根离子电离且和氢离子结合生成氢氧化铝白色沉淀,无气体放出,故A错误;
B.由电荷守恒可知,NaI溶液中c(Na+)+c(H+)=c(Cl-)+c(OH-),NaClO溶液中c(Na+)+c(H+)=c(ClO-)+c(OH-),NaCl溶液呈中性,NaClO溶液呈碱性,则NaClO溶液中c(H+)较小,则NaCl溶液中离子的总浓度大于NaClO溶液中离子的总浓度,故B正确;
C.盐溶液呈酸性,可能有两种情况,一是水解呈酸性,如氯化铵为强酸弱碱盐,水解呈酸性,二是酸式盐,如NaHSO4在水中电离出钠离子和硫酸根离子和氢离子,NaHSO4═Na++H++SO42-,呈酸性,故C错误;
D.盐酸抑制了水的电离,而氯化铵溶液中铵离子水解,促进了水的电离,所以两溶液中水的电离程度不相同,故D错误;
故选B.
B.由电荷守恒可知,NaI溶液中c(Na+)+c(H+)=c(Cl-)+c(OH-),NaClO溶液中c(Na+)+c(H+)=c(ClO-)+c(OH-),NaCl溶液呈中性,NaClO溶液呈碱性,则NaClO溶液中c(H+)较小,则NaCl溶液中离子的总浓度大于NaClO溶液中离子的总浓度,故B正确;
C.盐溶液呈酸性,可能有两种情况,一是水解呈酸性,如氯化铵为强酸弱碱盐,水解呈酸性,二是酸式盐,如NaHSO4在水中电离出钠离子和硫酸根离子和氢离子,NaHSO4═Na++H++SO42-,呈酸性,故C错误;
D.盐酸抑制了水的电离,而氯化铵溶液中铵离子水解,促进了水的电离,所以两溶液中水的电离程度不相同,故D错误;
故选B.
点评:本题考查了多元酸根的电离、离子浓度大小比较、盐类水解、水的电离等知识,侧重于学生的分析能力的考查,为高考常见题型,注意把握盐类水解和弱电解质的电离特点,题目难度中等.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
由乙醇制取乙二酸乙二酯,最简便的流程途径顺序正确的是( )
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应⑦中和反应 ⑧缩聚反应.
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应⑦中和反应 ⑧缩聚反应.
| A、⑤②①③⑥ |
| B、①②③④⑤⑦ |
| C、⑤②①③⑧ |
| D、①②⑤③⑥ |
配制500mL 1mol/LHCl溶液时,不需要的仪器是( )
| A、容量瓶(500mL) |
| B、分液漏斗 |
| C、烧杯 |
| D、胶头滴管 |
按如图所示装置进行下列不同的操作,其中不正确的是( )
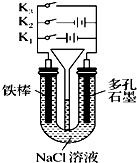

| A、只接通K1,一段时间后,U形管中出现白色沉淀 |
| B、只接通K2,U形管左、右两端液面均下降 |
| C、若U形管左、右两端上方充入一些空气,铁腐蚀的速度由大到小的顺序是:只接通K1>只接通K3>都断开>只接通K2 |
| D、若将氯化钠溶液改为氢氧化钠溶液,铁棒改为多孔石墨,先只接通K2,一段时间后,漏斗内液面上升,然后再只接通K3,则接通K3后装置中无电流通过 |
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、0.1 mol?L-1 NaHB溶液 pH=4,则溶液中:c(HB-)>c(B2-)>c(H2B) |
| B、0.1 mol?L-1 (NH4)2Fe(SO4)2溶液中:c(NH4+)+c(Fe2+)=0.3 mol?L-1 |
| C、NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| D、Na2CO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Na+) |